题目内容
17.质量分数为11.6%的某饱和一元醛水溶液5g,跟足量新制的Cu(OH)2悬浊液反应,生成Cu2O1.44g.通过计算推导出该有机物的分子式并写出其结构简式.分析 饱和一元醛与新制的Cu(OH)2悬浊液反应的化学方程式为R-CHO+2Cu(OH)2$\stackrel{△}{→}$R-COOH+Cu2O+2H2O,醛的质量为11.6%×5g=0.58g,n(Cu2O)=$\frac{1.44g}{144g/mol}$=0.01mol,结合反应的方程式计算.
解答 解:质量分数为11.6%的某饱和一元醛水溶液5g,醛的质量为11.6%×5g=0.58g,n(Cu2O)=$\frac{1.44g}{144g/mol}$=0.01mol,
则R-CHO+2Cu(OH)2$\stackrel{△}{→}$R-COOH+Cu2O+2H2O
1mol 1mol
n 0.01mol
n=0.01mol,
所以醛的相对分子质量为:$\frac{0.58g}{0.01mol}$=58,
则该有机物的分子式为C3H6O,结构简式为CH3CH2CHO,
答:该有机物的分子式为C3H6O,结构简式为CH3CH2CHO.
点评 本题考查有机物的推断及计算,为高频考点,侧重于学生的分析能力的考查,注意把握反应的方程式,为解答该题的关键,难度不大.

练习册系列答案
相关题目
7.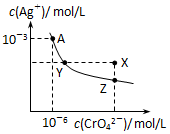 已知T℃时AgCl的Ksp=2×10-10;Ag2CrO4是一种橙红色固体,T℃时在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
已知T℃时AgCl的Ksp=2×10-10;Ag2CrO4是一种橙红色固体,T℃时在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
 已知T℃时AgCl的Ksp=2×10-10;Ag2CrO4是一种橙红色固体,T℃时在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
已知T℃时AgCl的Ksp=2×10-10;Ag2CrO4是一种橙红色固体,T℃时在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )| A. | T℃时Ag2CrO4的Ksp=2×10-12 | |
| B. | 浓度均为2×10-5mol/LAgNO3溶液与NaCl溶液等体积混合没有沉淀生成 | |
| C. | 在饱和Ag2CrO4溶液中加入K2CrO4固体可使溶液由Y点到X点 | |
| D. | 保持温度T℃不变,Ag2CrO4溶液长时间放置可使溶液由X点到Z点 |
8.一定温度和压强不变的条件下,发生可逆反应:A(g)+3B(g)?4C(g),下列叙述能作为该反应达到平衡状 态的标志的是( )
①混合气体平均摩尔质量不再变化
②v(A):v(B):v(C)=1:3:4
③A、B、C 的浓度不再变化
④C 的体积分数不再变化
⑤A、B、C 的分子数之比为 1:3:4
⑥混合气体的密度不再变化
⑦单位时间内消耗 amolA,同时生成 3amolB.
①混合气体平均摩尔质量不再变化
②v(A):v(B):v(C)=1:3:4
③A、B、C 的浓度不再变化
④C 的体积分数不再变化
⑤A、B、C 的分子数之比为 1:3:4
⑥混合气体的密度不再变化
⑦单位时间内消耗 amolA,同时生成 3amolB.
| A. | ③④⑦ | B. | ③④⑤⑥⑦ | C. | ②③④⑦ | D. | ①③⑤⑥⑦ |
5.下列各组溶液,不加其他试剂就能鉴别的是( )
| A. | Na2CO3、H2SO4、HCl、NaNO3 | B. | NaOH、NaCl、K2SO4、FeCl3 | ||
| C. | HCl、AgNO3、HNO3、MgCl2 | D. | K2SO4、Na2CO3、BaCl2、HNO3 |
2.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol•L-1 NaOH溶液中Na+的数目为0.1 NA | |
| B. | 标准状况下,2.24 L CCl4中的分子数目为0.1 NA | |
| C. | 0.1 mol Na2O2与足量CO2反应转移的电子数目为0.1 NA | |
| D. | 3.2 g O2和O3的混合物含有的分子数目为0.1 NA |
6.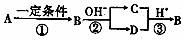 化合物A、B、C、D中均含有短周期元素X,B是一种常见的单质,它们有如图5所示的转化关系(部分产物与反应条件已略去),下列说法正确的是
化合物A、B、C、D中均含有短周期元素X,B是一种常见的单质,它们有如图5所示的转化关系(部分产物与反应条件已略去),下列说法正确的是
( )
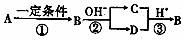 化合物A、B、C、D中均含有短周期元素X,B是一种常见的单质,它们有如图5所示的转化关系(部分产物与反应条件已略去),下列说法正确的是
化合物A、B、C、D中均含有短周期元素X,B是一种常见的单质,它们有如图5所示的转化关系(部分产物与反应条件已略去),下列说法正确的是( )
| A. | X元素可能是金属,也可能是非金属 | |
| B. | 反应①、②、③均为氧化还原反应 | |
| C. | 反应②、③为可逆反应 | |
| D. | 若B为金属单质,反应①的“一定条件”为电解时,通常加入冰晶石作为助溶剂 |
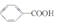 )和石灰的混合物得到一种液体,命名为苯.写出苯甲酸钠(
)和石灰的混合物得到一种液体,命名为苯.写出苯甲酸钠(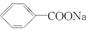 )与NaOH、生石灰共热生成苯的化学方程式:
)与NaOH、生石灰共热生成苯的化学方程式: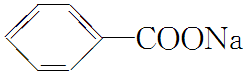 +NaOH
+NaOH  +Na2CO3.
+Na2CO3.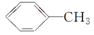 来制取
来制取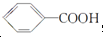 需要的试剂是KMnO4酸性溶液,下列物质属于苯的同系物且能被该试剂氧化的是d.
需要的试剂是KMnO4酸性溶液,下列物质属于苯的同系物且能被该试剂氧化的是d.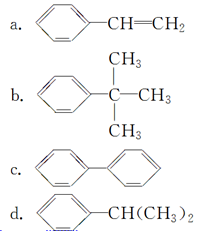
 .
.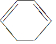 )脱去2mol氢原子变成苯却要放热,可推断苯比1,3-环己二烯稳定(填“稳定”或“不稳定”).
)脱去2mol氢原子变成苯却要放热,可推断苯比1,3-环己二烯稳定(填“稳定”或“不稳定”).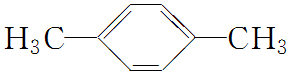 .
.