题目内容
aLFe2(SO4)3溶液中含Fe3+bg,则溶液中SO42-的物质的量浓度为( )mol/L.
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:根据n=
计算Fe3+的物质的量,1mol硫酸铁电离得到2molFe3+、3molSO42-,则溶液中n(SO42-)=
(Fe3+),再根据c=
计算SO42-的物质的量浓度.
| m |
| M |
| 3 |
| 2 |
| n |
| V |
解答:
解:bg Fe3+的物质的量为
=
mol,1mol硫酸铁电离得到2molFe3+、3molSO42-,则溶液中n(SO42-)=
(Fe3+)=
×
mol=
mol,则SO42-的物质的量浓度为
=
mol/L,
故选C.
| bg |
| 56g/mol |
| b |
| 56 |
| 3 |
| 2 |
| 3 |
| 2 |
| b |
| 56 |
| 3b |
| 112 |
| ||
| aL |
| 3b |
| 112a |
故选C.
点评:本题考查物质的量浓度的计算,难度不大,注意化学式意义及有关物质的量的计算公式的运用.

练习册系列答案
相关题目
下列实验方法或操作:
①用100mL筒量配制60mL10% 的盐酸;②称量没有腐蚀性固体药品时,把药品放在托盘上称量;③浓硫酸沾到皮肤上要先用抹布擦再用大量水冲洗;④用托盘天平称取5.20gNaCl晶体;⑤蒸馏开始时应先加热在开冷凝水;⑥萃取操作时选择的萃取剂的密度不必比水大;⑦用容量瓶配制一定浓度的某溶液后,将溶液保存在容量瓶中并贴上标签.其中正确的是( )
①用100mL筒量配制60mL10% 的盐酸;②称量没有腐蚀性固体药品时,把药品放在托盘上称量;③浓硫酸沾到皮肤上要先用抹布擦再用大量水冲洗;④用托盘天平称取5.20gNaCl晶体;⑤蒸馏开始时应先加热在开冷凝水;⑥萃取操作时选择的萃取剂的密度不必比水大;⑦用容量瓶配制一定浓度的某溶液后,将溶液保存在容量瓶中并贴上标签.其中正确的是( )
| A、③⑥ | B、②③⑦ |
| C、①③⑥ | D、③⑤⑥ |
下列关于钠的叙述中不正确的是( )
| A、钠具有很强的还原性 |
| B、钠原子的最外层只有一个电子 |
| C、在实验室中,钠通常保存在石蜡油或煤油中 |
| D、钠在常温下不易被氧化 |
在电解质溶液的导电性装置中,若向某一电解质溶液中逐滴加入另一种溶液,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
| A、将浓盐酸逐滴加入食盐溶液 |
| B、将硫酸逐滴加入氢氧化钡溶液 |
| C、将硫酸逐滴加入氢氧化钠溶液 |
| D、将浓盐酸逐滴加入氢氧化钠溶液 |
N2O俗称“笑气”,曾用作可吸入性麻醉剂.用以下反应可制取N2O:CO+NO2→CO2+N2O.下列说法正确的是( )
| A、反应中每生成1 mol N2O,消耗1.5 mol CO |
| B、等物质的量的N2O和CO2含有相等的电子数 |
| C、N2O只具有氧化性,无还原性 |
| D、反应中每生成1 mol N2O,电子转移的物质的量为3 mol |
水的电离过程为H2O?H++OH-,在25℃时水的离子积为KW=1.0×10-14,在35℃时水的离子积为KW=2.1×10-14,则下列叙述正确的是( )
| A、c(H+)随着温度的升高而降低 |
| B、35℃时c(H+)>c(OH-) |
| C、35℃时的水比25℃时的水电离程度小 |
| D、水的电离是个吸热过程 |
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
| A、HClO的结构式:H-Cl-O | ||
B、Na2O2的电子式: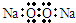 | ||
C、中子数为20的氯原子:
| ||
D、铝原子的结构示意图 |
已知化学反应2C(s)+O2(g)═2CO(g),2CO(g)+O2(g)=2CO2(g)都是放热反应.据此判断,下列说法中不正确的是( )
| A、1.2gC所具有的能量一定高于28gCO所具有的能量 |
| B、56g CO和32g O2所具有的总能量大于88g CO2所具有的总能量 |
| C、12g C和32g O2所具有的总能量大于44g CO2所具有的总能量 |
| D、将一定质量的C燃烧,生成CO2比生成CO时放出的热量多 |
某无色溶液中只可能溶有NH4+、K+、Al3+、Mg2+、HCO3-、Cl-、I-、MnO4-、SO42-等离子中的几种离子.分析其组成,现进行如下实验:
①取l0mL该溶液于试管中滴加足量的Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03mol白色沉淀甲.
②取上述反应后的滤液,加入AgNO3溶液未见沉淀产生.
③另取l0mL该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当加人NaOH的物质的量为0.03mol时,沉淀的量达到最大;继续滴加NaOH溶液并加热,开始产生气体丙,收集气体丙,体积换算成标况下为0.224L(假设丙全部逸出),最后沉淀完全溶解.下列推断正确的是( )
①取l0mL该溶液于试管中滴加足量的Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03mol白色沉淀甲.
②取上述反应后的滤液,加入AgNO3溶液未见沉淀产生.
③另取l0mL该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当加人NaOH的物质的量为0.03mol时,沉淀的量达到最大;继续滴加NaOH溶液并加热,开始产生气体丙,收集气体丙,体积换算成标况下为0.224L(假设丙全部逸出),最后沉淀完全溶解.下列推断正确的是( )
| A、肯定有K+、Al3+、Mg2+、SO42- |
| B、肯定有K+、NH4+、Al3+、SO42- |
| C、肯定没有K+、HCO3-、MnO4- |
| D、肯定没有K+、NH4+、Cl- |