题目内容
已知化学反应2C(s)+O2(g)═2CO(g),2CO(g)+O2(g)=2CO2(g)都是放热反应.据此判断,下列说法中不正确的是( )
| A、1.2gC所具有的能量一定高于28gCO所具有的能量 |
| B、56g CO和32g O2所具有的总能量大于88g CO2所具有的总能量 |
| C、12g C和32g O2所具有的总能量大于44g CO2所具有的总能量 |
| D、将一定质量的C燃烧,生成CO2比生成CO时放出的热量多 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:根据放热反应中反应物总能量大于生成物总能量,等量的物质完全燃烧时放出的热量大于不完全燃烧时的热量,据此来解答.
解答:
解:A、因2C+O2=2CO是放热反应,所以12gC和16gO2所具有的总能量一定高于28gCO所具有的能量,故A错误;
B、因2CO+O2═2CO2是放热反应,所以56gCO和32gO2所具有的总能量大于88gCO2所具有的总能量,即反应物的总能量大于生成物的总能量,故B正确;
C、因2C+O2=2CO,2CO+O2═2CO2都是放热反应,所以C+O2=CO2也是放热反应,所以12gC和32O2所具有的总能量一定高于44gCO2所具有的总能量,故C正确;
D、因物质完全燃烧放出的热量比不完全燃烧放出热量多,所以一定质量的碳燃烧,生成CO2比生成CO时放出的热量多,故D正确;
故选A.
B、因2CO+O2═2CO2是放热反应,所以56gCO和32gO2所具有的总能量大于88gCO2所具有的总能量,即反应物的总能量大于生成物的总能量,故B正确;
C、因2C+O2=2CO,2CO+O2═2CO2都是放热反应,所以C+O2=CO2也是放热反应,所以12gC和32O2所具有的总能量一定高于44gCO2所具有的总能量,故C正确;
D、因物质完全燃烧放出的热量比不完全燃烧放出热量多,所以一定质量的碳燃烧,生成CO2比生成CO时放出的热量多,故D正确;
故选A.
点评:本题考查了放热反应,解此类题要明确,反应物能量是指所有反应物的总能量和,生成物能量是指所有生成物总能量和,而不是某一个反应物和某一个生成物能量进行对比.

练习册系列答案
相关题目
aLFe2(SO4)3溶液中含Fe3+bg,则溶液中SO42-的物质的量浓度为( )mol/L.
A、
| ||
B、
| ||
C、
| ||
D、
|
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、1molNa2O和Na2O2混合物中含阴离子的总数为NA |
| B、标准状况下,22.4 LCCl4含CCl4分子为NA |
| C、1mol H3O+含质子数为10 NA |
| D、1 L0.1 mol?L-1的CuCl2溶液中含Cu2+为0.1NA |
在x R2++y H++O2=z R3++n H2O的离子反应中,化学计量系数z值为( )
| A、x | ||
| B、2 | ||
C、
| ||
| D、4 |
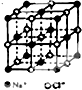 氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示.
氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示.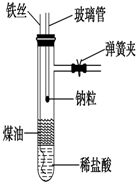 (1)按图所示组装仪器,向一支小的具支试管中加入2mL左右的稀盐酸,再加入2mL左右的煤油,玻璃管下端粘住钠粒(用滤纸吸干表面煤油,切去氧化层).
(1)按图所示组装仪器,向一支小的具支试管中加入2mL左右的稀盐酸,再加入2mL左右的煤油,玻璃管下端粘住钠粒(用滤纸吸干表面煤油,切去氧化层).