题目内容
下列图象不符合事实是( )
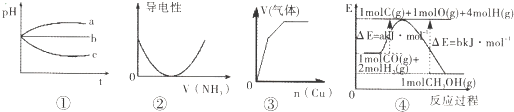

| A、图①:pH相同的H2S溶液、稀H2SO4溶液、H2SO3溶液露置于空气中一段时间后,溶液的pH随时间的变化情况 |
| B、图②:表示向乙酸溶液中通入NH3过程中溶液导电性的变化 |
| C、图③:将铜粉加入到一定量浓硝酸中产生的气体与加入铜量的变化情况 |
| D、图④知合成甲醇的热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=-(b-a)kJ?mol-1 |
考点:弱电解质在水溶液中的电离平衡,反应热和焓变,电解质溶液的导电性
专题:图示题
分析:A.pH相同的三种酸性溶液,由图象可知,a的pH变大,b的pH不变,c的pH减小,则露置于空气中一段时间,a可能被氧化,b为不挥发的强酸,c中氢离子浓度增大,以此来解答;
B.乙酸为弱电解质,与氨气反应生成醋酸铵为强电解质;
C.Cu与浓硝酸反应生成二氧化氮,与稀硝酸反应生成NO;
D.△H=正反应的活化能-逆反应的活化能.
B.乙酸为弱电解质,与氨气反应生成醋酸铵为强电解质;
C.Cu与浓硝酸反应生成二氧化氮,与稀硝酸反应生成NO;
D.△H=正反应的活化能-逆反应的活化能.
解答:
解:A.H2S溶液被氧化生成水和S,其pH增大,稀H2SO4溶液不发生变化,其pH不变,而H2SO3溶液被氧化生成硫酸,氢离子浓度增大,其pH减小,与图象一致,故A正确;
B.乙酸为弱电解质,溶液的导电能力较弱,与氨气反应生成醋酸铵为强电解质,溶液的导电能力增强,图中曲线变化趋势错误,故B错误;
C.铜先和浓硝酸反应生成二氧化氮气体,随着反应的进行,浓硝酸变成稀硝酸,铜和稀硝酸反应生成一氧化氮,当硝酸完全反应时,生成的气体为定值,故C正确;
D.△H=正反应的活化能-逆反应的活化能,则合成甲醇的热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=-(b-a)kJ?mol-1,故D正确.
故选B.
B.乙酸为弱电解质,溶液的导电能力较弱,与氨气反应生成醋酸铵为强电解质,溶液的导电能力增强,图中曲线变化趋势错误,故B错误;
C.铜先和浓硝酸反应生成二氧化氮气体,随着反应的进行,浓硝酸变成稀硝酸,铜和稀硝酸反应生成一氧化氮,当硝酸完全反应时,生成的气体为定值,故C正确;
D.△H=正反应的活化能-逆反应的活化能,则合成甲醇的热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=-(b-a)kJ?mol-1,故D正确.
故选B.
点评:本题考查了图象的分析和应用,涉及元素化合物的性质、溶液的导电性、反应热等,题目难度不大,侧重于考查学生的读图能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列分离或提纯物质的方法正确的是( )
| A、用渗析的方法精制Fe(OH)3胶体 |
| B、用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 |
| C、用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
| D、用加热蒸发结晶的方法从AlCl3溶液得到AlCl3 |
下列各组离子中,能在无色溶液中大量共存的是( )
| A、H+、Ca2+、Cl-、CO32- |
| B、NO3-、Cl-、K+、H+ |
| C、Na+、Fe3+、SO42-、OH- |
| D、Na+、Cu2+、Cl-、SO42- |
下列能说明可逆反应2A(g)+B(g)?2C(g)+D(g)在一定条件下已达到化学平衡状态的事实是( )
| A、容器内压强不随时间的变化而变化 |
| B、容器内A、B、C、D四者共存 |
| C、C的生成速率是D的生成速率的两倍 |
| D、A的消耗速率是D的消耗速率的两倍 |
在298K时,2SO2(g)+O2(g)?2SO3(g)△H=-197kJ?mol-1,在相同的温度下,向密闭真空容器中通入2molSO2和1molO2,达到平衡时放出热量Q1; 向另一个同体积的密闭真空容器中通入1molSO2和0.5molO2,达到平衡时放出热量Q2,则下列关系中正确的是( )
A、Q2<
| ||
B、Q2=
| ||
C、Q2>
| ||
| D、Q1=Q2=197kJ |
下列描述中正确的是( )
| A、已知C(金刚石,s)=C(石墨,s)△H<0,则金刚石比石墨稳定 |
| B、CO(g)的燃烧热是283.0 kJ?mol-1,则2CO2(g)=2CO(g)+O2(g)的△H=2×(+283.0)kJ?mol-1 |
| C、HCl和NaOH反应的中和热△H=-57.3 kJ?mol-1,则H2SO4和Ba(OH)2的反应热△H=2×(-57.3)kJ?mol-1 |
| D、1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |