题目内容
下列有关元素周期表和元素周期律的说法中,正确的是( )
| A、第三周期主族元素中氯的原子半径最大 |
| B、原子最外层电子数为2的元素一定位于周期表中的第ⅡA族 |
| C、同主族自上而下,其非金属元素气态氢化物的稳定性逐渐增强 |
| D、镓(Ga)位于第4周期、ⅢA族,其最高价氧化物对应水化物的化学式为Ga(OH)3 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:A.同周期自左而右原子半径减小;
B.原子最外层电子数为2的元素可以为He、Mg、Zn等;
C.同主族自上而下元素非金属性减弱,而非金属性越强氢化物越稳定;
D.镓(Ga)位于第4周期ⅢA族,最高正化合价为+3,结合氢氧化铝书写其氢氧化物化学式.
B.原子最外层电子数为2的元素可以为He、Mg、Zn等;
C.同主族自上而下元素非金属性减弱,而非金属性越强氢化物越稳定;
D.镓(Ga)位于第4周期ⅢA族,最高正化合价为+3,结合氢氧化铝书写其氢氧化物化学式.
解答:
解:A.同周期自左而右原子半径减小,第三周期主族元素中氯的原子半径最小,Na原子半径最大,故A错误;
B.原子最外层电子数为2的元素可以为He、Mg、Zn等,不一定处于ⅡA族,故B错误;
C.同主族自上而下元素非金属性减弱,其非金属元素气态氢化物的稳定性逐渐减弱,故C错误;
D.镓(Ga)位于第4周期ⅢA族,最高正化合价为+3,最高价氧化物对应水化物的化学式为Ga(OH)3,硅D正确,
故选D.
B.原子最外层电子数为2的元素可以为He、Mg、Zn等,不一定处于ⅡA族,故B错误;
C.同主族自上而下元素非金属性减弱,其非金属元素气态氢化物的稳定性逐渐减弱,故C错误;
D.镓(Ga)位于第4周期ⅢA族,最高正化合价为+3,最高价氧化物对应水化物的化学式为Ga(OH)3,硅D正确,
故选D.
点评:本题考查结构性质位置关系,难度不大,注意对元素周期律的理解掌握,注意元素周期表中特殊性.

练习册系列答案
相关题目
水是生命之源,下列关于水的说法正确的是( )
| A、海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等 |
| B、某温度下,pH=6的蒸馏水显酸性 |
| C、氯气有毒,因而自来水的杀菌消毒一定不能使用氯气 |
| D、明矾可用于水的净化与杀菌消毒 |
下列实验装置或实验操作使用正确的是( )
A、 |
B、 |
C、 |
D、 |
下列说法正确的是( )
| A、向饱和食盐水中先通足量CO2气体,再通入足量NH3,会析出NaHCO3晶体 |
| B、使用一定的催化剂可将汽车尾气中的CO和NO转化成CO2和N2 |
| C、将一定质量不同组成的铝钠合金投入足量盐酸中,铝的质量分数越小,放出的H2越多 |
| D、等质量的两份铝,分别和含n mol HCl和n mol NaOH 溶液反应,放出的气体的体积一定是NaOH溶液的多 |

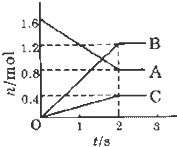 某温度下,在体积为5L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图所示,则该反应的化学方程式为
某温度下,在体积为5L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图所示,则该反应的化学方程式为