题目内容
(1)一瓶无色气体,可能含有CH4和CH2═CH2或其中的一种,与一瓶Cl2混合后光照,观察到黄绿色逐渐褪去,瓶壁有少量无色油状小液滴.
①由上述实验现象推断出该瓶气体中一定含有CH4,你认为是否正确,为什么?
②上述实验中可能涉及的反应类型有
(2)含有C═C的化合物与CH2═CH2一样,在一定条件下可聚合成高分子化合物.
①广泛用作农用薄膜的聚氯乙烯塑料,是由 聚合而成的,其化学方程式是
聚合而成的,其化学方程式是
②电器包装中大量使用的泡沫塑料的主要成分是聚苯乙烯(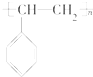 ),它是由 (写结构简式)聚合而成.
),它是由 (写结构简式)聚合而成.
①由上述实验现象推断出该瓶气体中一定含有CH4,你认为是否正确,为什么?
②上述实验中可能涉及的反应类型有
(2)含有C═C的化合物与CH2═CH2一样,在一定条件下可聚合成高分子化合物.
①广泛用作农用薄膜的聚氯乙烯塑料,是由
 聚合而成的,其化学方程式是
聚合而成的,其化学方程式是②电器包装中大量使用的泡沫塑料的主要成分是聚苯乙烯(
 ),它是由
),它是由考点:有机物的结构和性质,有机物的鉴别
专题:有机反应,有机物的化学性质及推断
分析:(1)乙烯和氯气发生加成反应,甲烷和氯气发生取代反应;
(2)CH2═CHCl含有碳碳双键,可发生加聚反应生成聚氯乙烯,聚苯乙烯的单体为苯乙烯.
(2)CH2═CHCl含有碳碳双键,可发生加聚反应生成聚氯乙烯,聚苯乙烯的单体为苯乙烯.
解答:
解:(1)①因为CH2=CH2也可以与Cl2发生加成反应,而使黄绿色逐渐褪色,生成的CH2ClCH2Cl也是油状液体,则不能确定是否含有甲烷,
故答案为:不正确,因为CH2=CH2也可以与Cl2发生加成反应,而使黄绿色逐渐褪色,生成的CH2ClCH2Cl也是油状液体;
②乙烯和氯气发生加成反应,甲烷和氯气发生取代反应;故答案为:取代反应,加成反应;
(2)①由氯乙烯合成聚氯乙烯的反应为: ,
,
故答案为: ;
;
②合成聚苯乙烯的单体是苯乙烯,即 ,故答案为:
,故答案为: .
.
故答案为:不正确,因为CH2=CH2也可以与Cl2发生加成反应,而使黄绿色逐渐褪色,生成的CH2ClCH2Cl也是油状液体;
②乙烯和氯气发生加成反应,甲烷和氯气发生取代反应;故答案为:取代反应,加成反应;
(2)①由氯乙烯合成聚氯乙烯的反应为:
 ,
,故答案为:
 ;
;②合成聚苯乙烯的单体是苯乙烯,即
 ,故答案为:
,故答案为: .
.
点评:本题综合考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质以及高聚物单体的判断,难度中等.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
由CH4、CO、H2中的一种、两种或三种组成的气体,完全燃烧后,生成的CO2和H2O的物质的量之比是1:2,下列判断中不正确的是( )
| A、原气体中一定含有CH4 |
| B、原气体中可能不含CH4 |
| C、原气体中若含有CO,则一定含有H2 |
| D、气体中若同时含有CH4、CO和H2,则CO与H2的物质的量之比为1:2 |
X元素的阳离子和Y元素的阴离子具有与氩原子相同的电子层结构,下列叙述中正确的是( )
| A、X的质子数比Y的小 |
| B、X原子的最外层电子数比Y的大 |
| C、X元素的最高正价比Y的小 |
| D、X是非金属元素,而Y是金属元素 |
为了除去粗盐中的Ca2+、Mg2+、SO
可将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量氢氧化钠;③加适量盐酸;④加足量碳酸钠溶液;⑤加过量氯化钡溶液.下列操作顺序正确的是( )
2- 4 |
| A、①④②⑤③ |
| B、④①②⑤③ |
| C、④②⑤①③ |
| D、⑤②④①③ |
将0.1mol/L的HCl和0.06mol/L的Ba(OH)2溶液以等体积混合后,该混合溶液的pH是( )
| A、1.7 | B、12.3 |
| C、12 | D、2 |
在恒温恒压下,向密闭容器中充入4molSO2和2molO2,发生如下反应:2SO2(g)+O2(g)?2SO3(g)△H<0.2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量Q kJ,则下列分析正确的是( )
| A、在该条件下,反应前后的压强之比为6:5.3 |
| B、若反应开始时容器体积为2L,则v(SO3)=0.35mol/(L?min) |
| C、若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)<1.4mol |
| D、若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量大于Q kJ |
在相同温度下,两个反应放出的热量分别用Q1和Q2表示,H2(g)+
O2(g)=H2O(g);△H=-Q1 kJ?mol-1;2H2(g)+O2(g)=2H2O(l);△H=-Q2 kJ?mol-1,则下列关系正确的是( )
| 1 |
| 2 |
| A、Q1<2Q2 |
| B、2Q1=Q2 |
| C、2Q1<Q2 |
| D、2Q1>Q2 |