题目内容
在相同温度下,两个反应放出的热量分别用Q1和Q2表示,H2(g)+
O2(g)=H2O(g);△H=-Q1 kJ?mol-1;2H2(g)+O2(g)=2H2O(l);△H=-Q2 kJ?mol-1,则下列关系正确的是( )
| 1 |
| 2 |
| A、Q1<2Q2 |
| B、2Q1=Q2 |
| C、2Q1<Q2 |
| D、2Q1>Q2 |
考点:反应热的大小比较
专题:
分析:H2O(g)=H2O(l);△H<0,利用盖斯定律进行判断.
解答:
解:已知H2O(g)=H2O(l);△H<0,
则有H2O(g)=H2O(l);△H=(-Q2kJ/mol)-2(-Q1kJ/mol)<0,
可得2Q1<Q2.故选C.
则有H2O(g)=H2O(l);△H=(-Q2kJ/mol)-2(-Q1kJ/mol)<0,
可得2Q1<Q2.故选C.
点评:本题考查反应的比较问题,题目难度不大,注意气态水生成液态水为放热过程,利用盖斯定律比较反应热的大小.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
对于反应M+N→P,如果温度每升高10℃,化学反应速度增大为原来的3倍,在10℃时,完成反应10%需81min,则在30℃时完成反应10%需要时间为( )
| A、27min |
| B、9min |
| C、13.5min |
| D、3min |
通常用来衡量一个国家石油化工发展水平标志的是( )
| A、甲烷的产量 | B、乙烯的产量 |
| C、乙醇的产量 | D、苯的产量 |
下列说法正确的是( )
| A、水玻璃显碱性,滴入酚酞呈现红色 |
| B、工艺师利用盐酸刻蚀玻璃制作艺术品 |
| C、水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| D、单质硅是制造光导纤维的主要材料 |
 在如图所示装置中进行氨的催化氧化实验:往三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶中并接近液面.反应过程中,可观察到瓶中有红棕色气体产生,铂丝始终保持红热.下列有关说法错误的是( )
在如图所示装置中进行氨的催化氧化实验:往三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶中并接近液面.反应过程中,可观察到瓶中有红棕色气体产生,铂丝始终保持红热.下列有关说法错误的是( )A、反应后溶液中含有NO
| ||
| B、反应后溶液的PH值增大 | ||
| C、实验过程中有化合反应发生 | ||
| D、实验过程中铂丝始终保持红热,说明反应是放热反应 |
X、Y、Z、M 是元素周期表中前20 号元素,其原子序数依次增大,Y与X、Z 相邻.X 的核电荷数是Y 的核外电子数的一半,Y与M 可形成化合物M2Y.下列说法正确的是( )
| A、稳定性:X 的氢化物>Y 的氢化物>Z 的氢化物 |
| B、简单离子的半径:M的离子>Z 的离子>Y 的离子>X的离子 |
| C、YX2、M2Y 都是含有极性键的极性分子 |
| D、Z元素的最高价氧化物的水化物的化学式为HZO4 |
W、X、Y、Z是核外电子层数相同且原子序数依次增大的短周期元素,W、X是金属元素,Y的氢化物为H2Y,Z的某种含氧酸有漂白性.W、X的最高价氧化物对应的水化物可以发生反应生成盐和水.下列判断正确的是( )
| A、X的金属性强于W的金属性 |
| B、W、X分别与Z形成的化合物都是离子化合物 |
| C、W、X、Y、Z的简单离子的半径:Y>Z>W>X |
| D、Y的氧化物通入含有Z单质的溶液中,一定无明显变化 |
 聚合而成的,其化学方程式是
聚合而成的,其化学方程式是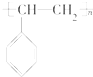 ),它是由
),它是由