题目内容
X元素的阳离子和Y元素的阴离子具有与氩原子相同的电子层结构,下列叙述中正确的是( )
| A、X的质子数比Y的小 |
| B、X原子的最外层电子数比Y的大 |
| C、X元素的最高正价比Y的小 |
| D、X是非金属元素,而Y是金属元素 |
考点:原子结构与元素的性质
专题:元素周期律与元素周期表专题
分析:X元素的阳离子和Y元素的阴离子具有与氩原子相同的电子层结构,则X元素位于第四周期、Y位于第三周期,原子序数X>Y,
A.原子中质子数=原子序数;
B.金属元素最外层电子数在1-2之间,非金属元素最外层电子数在3-7之间;
C.主族元素最外层电子数等于其最高化合价(O、F元素除外);
D.金属元素能形成简单阳离子、非金属元素能形成简单阴离子.
A.原子中质子数=原子序数;
B.金属元素最外层电子数在1-2之间,非金属元素最外层电子数在3-7之间;
C.主族元素最外层电子数等于其最高化合价(O、F元素除外);
D.金属元素能形成简单阳离子、非金属元素能形成简单阴离子.
解答:
解:X元素的阳离子和Y元素的阴离子具有与氩原子相同的电子层结构,则X元素位于第四周期、Y位于第三周期,原子序数X>Y,X为金属元素、Y为非金属元素,
A.原子中质子数=原子序数,所以X的质子数大于Y,故A错误;
B.金属元素最外层电子数在1-2之间,非金属元素最外层电子数在3-7之间,所以X元素的最外层电子数小于Y,故B错误;
C.主族元素最外层电子数等于其最高化合价(O、F元素除外),金属元素最外层电子数在1-2之间,非金属元素最外层电子数在3-7之间,X为金属元素、Y为非金属元素,所以X元素的最高正价比Y小,故C正确;
D.金属元素能形成简单阳离子、非金属元素能形成简单阴离子,所以X为金属元素、Y为非金属元素,故D错误;
故选C.
A.原子中质子数=原子序数,所以X的质子数大于Y,故A错误;
B.金属元素最外层电子数在1-2之间,非金属元素最外层电子数在3-7之间,所以X元素的最外层电子数小于Y,故B错误;
C.主族元素最外层电子数等于其最高化合价(O、F元素除外),金属元素最外层电子数在1-2之间,非金属元素最外层电子数在3-7之间,X为金属元素、Y为非金属元素,所以X元素的最高正价比Y小,故C正确;
D.金属元素能形成简单阳离子、非金属元素能形成简单阴离子,所以X为金属元素、Y为非金属元素,故D错误;
故选C.
点评:本题考查原子结构和元素性质,侧重考查分析、推断能力,知道元素周期表结构、原子结构、元素性质即可解答,熟练掌握元素周期表中元素之间关系,题目难度中等.

练习册系列答案
相关题目
电子数相等的粒子叫做等电子体,下列各组粒子属于等电子体是( )
| A、CO和CO2 |
| B、NO和NO2 |
| C、CH4和NH3 |
| D、CO2和SO2 |
下列关于1-20号元素的原子结构的有关说法正确的( )
| A、离子的最外层电子数比其次外层电子数多的元素一定是第二周期的元素 |
| B、元素形成的简单离子中,最外层电子数一定是8或2 |
| C、最外层电子数与次外层电子数相等的离子一定是第三周期的非金属元素 |
| D、原子得到电子成为阴离子时,电子层数一定不变,原子失去电子成为阳离子时,电子层数一定减少 |
下列说法中,正确的是( )
| A、可燃物的燃烧都是放热反应 |
| B、加热后才能发生的反应一定是吸热反应 |
| C、干冰升华时要吸收热量,所以这是吸热反应 |
| D、1 mol Ba(OH)2与1 mol H2SO4反应释放的热量为Q,则Q为它们反应的中和热 |
下列说法正确的是( )
| A、容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小 |
| B、配制溶液时,若在定容时仰视读数,会导致所配标准溶液的浓度偏大 |
| C、中和等体积、等物质的量的浓度的盐酸和醋酸所消耗的n(NaOH)相等 |
| D、25℃与60℃时,水的pH相等 |
 在如图所示装置中进行氨的催化氧化实验:往三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶中并接近液面.反应过程中,可观察到瓶中有红棕色气体产生,铂丝始终保持红热.下列有关说法错误的是( )
在如图所示装置中进行氨的催化氧化实验:往三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶中并接近液面.反应过程中,可观察到瓶中有红棕色气体产生,铂丝始终保持红热.下列有关说法错误的是( )A、反应后溶液中含有NO
| ||
| B、反应后溶液的PH值增大 | ||
| C、实验过程中有化合反应发生 | ||
| D、实验过程中铂丝始终保持红热,说明反应是放热反应 |




 聚合而成的,其化学方程式是
聚合而成的,其化学方程式是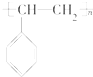 ),它是由
),它是由