题目内容
以下实验能达到目的是( )
| A、向已经变质的FeCl2溶液中滴加KSCN溶液,溶液变红,则说明FeCl2已完全变质 |
| B、向某一无色气体中通入氧气,气体变红棕色,则证明有NO |
| C、可用PH试纸来测浓硫酸的PH值 |
| D、取某溶液,先后滴入氯化钡溶液和稀硝酸,产生白色沉淀,则该溶液中一定含有SO42- |
考点:化学实验方案的评价
专题:实验评价题
分析:A.已经变质的FeCl2溶液中,混有铁离子;
B.NO为无色,二氧化氮为红棕色气体;
C.浓硫酸具有脱水性;
D.沉淀可能为AgCl.
B.NO为无色,二氧化氮为红棕色气体;
C.浓硫酸具有脱水性;
D.沉淀可能为AgCl.
解答:
解:A.已经变质的FeCl2溶液中,混有铁离子,滴加KSCN溶液,溶液变红,则说明FeCl2已完全变质,故A正确;
B.NO为无色,NO易被氧化生成红棕色的二氧化氮气体,则向某一无色气体中通入氧气,气体变红棕色,则证明有NO,故B正确;
C.浓硫酸具有脱水性,则不能利用pH试纸测定浓硫酸的pH,故C错误;
D.某溶液,先后滴入氯化钡溶液和稀硝酸,产生白色沉淀,沉淀可能为AgCl,也可能为硫酸钡,则溶液中可能含银离子或硫酸根离子,但二者不能同时存在,故D错误;
故选AB.
B.NO为无色,NO易被氧化生成红棕色的二氧化氮气体,则向某一无色气体中通入氧气,气体变红棕色,则证明有NO,故B正确;
C.浓硫酸具有脱水性,则不能利用pH试纸测定浓硫酸的pH,故C错误;
D.某溶液,先后滴入氯化钡溶液和稀硝酸,产生白色沉淀,沉淀可能为AgCl,也可能为硫酸钡,则溶液中可能含银离子或硫酸根离子,但二者不能同时存在,故D错误;
故选AB.
点评:本题考查化学实验方案的评价,为高频考点,把握离子的性质及离子的检验、pH的测定及物质的性质为解答的关键,注重实验技能的考查,注意实验的操作性和评价性分析,题目难度不大.

练习册系列答案
相关题目
已知短周期元素的离子:aA3+、bB2+、cC2-、dD-具有相同的电子层结构,下列关系错误的是( )
| A、质子数:b>C |
| B、原子半径:r(A)>r(D) |
| C、离子的还原性:C2->D- |
| D、离子半径:r(B2+)>r(C2-) |
下列事实不能用勒夏特列原理解释的是( )
| A、红棕色NO2加压后颜色先变深后变浅 |
| B、实验室中常用排饱和食盐水的方法收集氯气 |
| C、SO2催化氧化成SO3的反应,使用过量的空气以提高二氧化硫的利用率 |
| D、压缩H2与I2(g)反应的平衡混合气体,颜色变深 |
有机物的化学性质主要由其官能团决定.苹果酸是一种有机酸,结构简式为: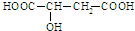 .下列有关苹果酸的说法不正确的是( )
.下列有关苹果酸的说法不正确的是( )
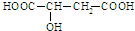 .下列有关苹果酸的说法不正确的是( )
.下列有关苹果酸的说法不正确的是( )| A、1mol苹果酸足量金属钠反应,生成氢气3g |
| B、1mol苹果酸与足量氢氧化钠溶液反应,消耗3mol氢氧化钠 |
| C、1mol苹果酸能与足量的碳酸氢钠溶液反应,标况下生成44.8L的二氧化碳气体 |
| D、苹果酸在一定条件下既能与醋酸反应,又能与乙醇反应,也可以自身发生酯化反应 |
下列排列有错误的是( )
| A、粒子半径:Al3+>Mg2+>Na+>F- |
| B、稳定性:HI<HBr<HCl<HF |
| C、酸性:H4SiO4<H3PO4<H2SO4<HClO4 |
| D、碱性:Al(OH)3<Mg(OH)2<Ca(OH)2<KOH |
下列有关物质浓度关系的描述中,正确的是( )
| A、25℃时,向0.1mol?L-1 NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) |
| B、25℃时,NaB溶液的pH=8,c(Na+)+c(B-)=9.9×10-7mol?L-1 |
| C、0.1mol?L-1的NaHCO3溶液中:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
| D、同温下,pH相同时,溶液物质的量浓度:c(CH3COONa)<c(NaHCO3)<c(C6H5ONa)<c(Na2CO3) |
下列各组元素按电负性大小排列正确的是( )
| A、F>N>O |
| B、O>Cl>F |
| C、As>P>H |
| D、Cl>S>As |
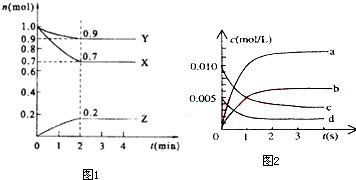
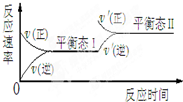 随着人类对温室效应和资源短缺等问题的重视,降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前有一种方法是用CO2来生产燃料甲醇CH3OH.在体积不变的5L密闭容器中,充入一定量的CO2和 H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);(正反应为放热反应)经过10min反应达到平衡,测得物质的浓度如下表所示.
随着人类对温室效应和资源短缺等问题的重视,降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前有一种方法是用CO2来生产燃料甲醇CH3OH.在体积不变的5L密闭容器中,充入一定量的CO2和 H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);(正反应为放热反应)经过10min反应达到平衡,测得物质的浓度如下表所示.