题目内容
6.火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,黑火药在发生爆炸时,发生如下的反应:S+2KNO3+3C═K2S+3CO2↑+N2↑;(1)用双线桥的方法标出化合价升降、电子得失数目情况:S+2KNO3+3C═K2S+3CO2↑+N2↑
(2)其中被还原的元素是N 和S,被氧化的元素是C;氧化剂是KNO3和S,还原剂是C;氧化产物是CO2,还原产物是K2S和N2(填元素符号或物质的化学式).
分析 反应2KNO3+3C+S=K2S+N2↑+3CO2↑中,N、S元素的化合价降低,C元素的化合价升高,含元素化合价降低的物质为氧化剂,氧化剂被还原,而含元素化合价升高的物质为还原剂,还原剂被氧化,对应的产物为氧化产物,结合化合价的变化计算转移电子数目.
解答 解:(1)在反应2KNO3+3C+S=K2S+N2↑+3CO2↑中,N元素的化合价由+5降低为0,S元素的化合价由0降低为-2价,C元素的化合价由0升高到+4,反应中转移电子数为4,则转移的电子方向和数目为 ,故答案为:
,故答案为: ;
;
(2)N元素的化合价由+5降低为0,S元素的化合价由0降低为-2价,则KNO3和S作氧化剂,被还原的元素为N、S,
C元素的化合价由0升高到+4,则C作还原剂,被氧化,对应的CO2为氧化产物,K2S和N2为还原产物,
故答案为:N 和S;C;KNO3和S;C;CO2;K2S和N2.
点评 本题考查氧化还原反应,侧重于学生的分析能力的考查,明确元素的化合价的变化及氧化还原反应中的基本概念是解答本题的关键,难度不大.

练习册系列答案
相关题目
16.下列现象因发生取代反应而产生的是( )
| A. | 甲烷与氯气混合,光照一段时间后黄绿色消失 | |
| B. | 将苯加入溴水中,振荡后水层接近无色 | |
| C. | 乙烯使溴的四氯化碳溶液褪色 | |
| D. | 乙烯使酸性高锰酸钾溶液褪色 |
17.氯碱工业是最基本的化学工业之一,它的产品除应用于化学工业本身外,还广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业.考虑到生产实际经济效益吸收氯碱工业的尾气氯气最好采用( )
| A. | 浓NaOH溶液 | B. | 饱和食盐水 | C. | 石灰乳 | D. | 浓硫酸 |
14.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 5.6gFe和足量的盐酸完全反应失去电子数为0.3 NA | |
| B. | 1.0mol•L的NaCl 溶液中Na+数为NA | |
| C. | 16gCH4所含的电子数为10NA | |
| D. | 标况下,4.48L的水中含有H2O分子的数目为0.2NA |
1.实验室制Cl2的反应如下:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,下列有关该反应的说法正确的是( )
| A. | MnO2是还原剂 | B. | HCl被氧化 | ||
| C. | MnO2发生氧化反应 | D. | 每反应4molHCl转移4mol电子 |
11.某烃0.5mol最多能和1mol HCl加成,生成氯代烃,此氯代烃l mol能和4mol Cl2发生取代反应,生成物中只有碳氯两种元素,此烃为( )
| A. | C2H2 | B. | C2H4 | C. | C3H4 | D. | C6H6 |
18.下列各醇,能发生催化氧化的是( )
| A. | 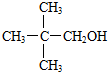 | B. |  | C. | 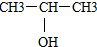 | D. | 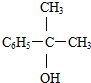 |
15.工业上用某矿渣(主要成分是Cu2O,少量杂质是Al2O3、Fe2O3和SiO2)提取铜的操作流程如下:
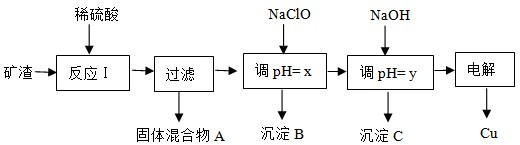
已知:Cu2O+2H+=Cu+Cu2++H2O
(1)固体混合物A中的成分是SiO2、Cu(填化学式).
(2)反应I完成后,铁元素的存在形式为Fe2+(填离子符号).
(3)y的数值范围是5.2≤pH<5.4.
(4)若电解法获得Cu 64.0g,则原矿渣中Cu2O的质量是c.
a、144.0gb、大于144.0g c、小于144.0g
(5)下列关于用NaClO调节溶液pH的说法正确的是b.
a、加入NaClO可使溶液的pH降低
b、NaClO能调节pH的主要原因是由于发生反应:ClO-+H+=HClO,ClO-消耗H+,从而达到调节pH的目的
c、NaClO能调节pH的主要原因是由于NaClO水解:ClO-+H2O?HClO+OH-消耗H+,从而达到调节pH的目的.
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,且该物质与还原产物的物质的量之比为4:1,该反应的离子方程式为2Fe2++5ClO-+5H2O=2Fe(OH)3+Cl-+4HClO.

已知:Cu2O+2H+=Cu+Cu2++H2O
| 沉淀 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 5.4 | 4.0 | 2.2 | 5.8 |
| 沉淀完成pH | 6.7 | 5.2 | 3.2 | 8.8 |
(2)反应I完成后,铁元素的存在形式为Fe2+(填离子符号).
(3)y的数值范围是5.2≤pH<5.4.
(4)若电解法获得Cu 64.0g,则原矿渣中Cu2O的质量是c.
a、144.0gb、大于144.0g c、小于144.0g
(5)下列关于用NaClO调节溶液pH的说法正确的是b.
a、加入NaClO可使溶液的pH降低
b、NaClO能调节pH的主要原因是由于发生反应:ClO-+H+=HClO,ClO-消耗H+,从而达到调节pH的目的
c、NaClO能调节pH的主要原因是由于NaClO水解:ClO-+H2O?HClO+OH-消耗H+,从而达到调节pH的目的.
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,且该物质与还原产物的物质的量之比为4:1,该反应的离子方程式为2Fe2++5ClO-+5H2O=2Fe(OH)3+Cl-+4HClO.