题目内容
13.醛可发生分子间的反应,生成烃基醛,如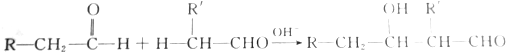
现在用甲醛和乙醛来制备季戊四醇[C(CH2OH)4],消耗的甲醛与乙醛的物质的量之比为( )
| A. | 3:1 | B. | 2:1 | C. | 4:1 | D. | 1:1 |
分析 由题目信息可知:3HCHO+CH3CHO→(HOCH2)3CCHO,(HOCH2)3CCHO再与氢气发生加成反应得到C(CH2OH)4.
解答 解:由题目信息可知:3HCHO+CH3CHO→(HOCH2)3CCHO,(HOCH2)3CCHO再与氢气发生加成反应得到C(CH2OH)4,故消耗的甲醛与乙醛的物质的量之比为3:1,
故选:A.
点评 本题考查有机物合成、化学方程式计算,关键是根据题目信息确定合成路线,难度中等.

练习册系列答案
相关题目
4.下列各项中物质的类别和用途对应关系不正确的是( )
| A | B | C | D |
| A12O3 | Si | Na2O2 | Na2SiO3 |
| 两性氧化物 | 单质 | 碱性氧化物 | 正盐 |
| 工业用电解法冶炼铝 | 制作太阳能电池 | 用于呼吸面具作为氧气的来源 | 制备硅胶 |
| A.A | B.B | C.C | D.D |
8.某元素的最高正价和最低负价的绝对值相等,其最高价氧化物的式量与其气态氢化物的式量之比是11:4,该元素的最高价氧化物形成的晶体是( )
| A. | 分子晶体 | B. | 离子晶体 | C. | 原子晶体 | D. | 以上晶体都不是 |
5.下列离子方程式正确的是( )
| A. | 硫酸铜和铝:2Al+3Cu2+═3Cu+2Al3+ | |
| B. | 氧化铜与盐酸反应:O2-+2H+═H2O | |
| C. | 碳酸钡与盐酸:CO32-+2H+═H2O+CO2↑ | |
| D. | Cu(OH)2加入H2SO4:2H++Cu(OH)2═Cu2++2H2O |
2.现将淀粉胶体和Na2SO4的混合溶液装在半透膜中,浸泡在盛蒸馏水的烧杯内,下列说法中能证明半透膜完好无损的是( )
| A. | 取烧杯内液体,加入BaCl2溶液产生白色沉淀 | |
| B. | 取烧杯内液体,加入碘水不变蓝 | |
| C. | 取半透膜内液体,加入BaCl2溶液没有白色沉淀 | |
| D. | 取半透膜内液体,加入碘水变蓝 |
3.化学无处不在,下列与化学有关的说法正确的是( )
| A. | SO2能漂白纸浆等,故可广泛用于食品的漂白. | |
| B. | 烹调鱼时加入少量料酒和食醋可以减少腥味、增加香味 | |
| C. | 工业上用电解熔融的AlCl3来制取铝单质 | |
| D. | 制作航天服的聚酯纤维和用于光纤通信的光导纤维都是新型无机非金属材料 |
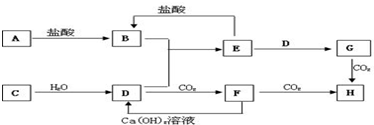
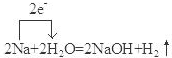 .
.