题目内容
8.某元素的最高正价和最低负价的绝对值相等,其最高价氧化物的式量与其气态氢化物的式量之比是11:4,该元素的最高价氧化物形成的晶体是( )| A. | 分子晶体 | B. | 离子晶体 | C. | 原子晶体 | D. | 以上晶体都不是 |
分析 元素的最高正价和最低负价的绝对值之和等于8,可知该元素最高正价为+4价,最低负价为-4价,因此其最高价氧化物和其气态氢化物的化学式可分别表示为XO2、XH4,然后根据式量比求出该元素的相对原子质量以确定该元素,最后根据该元素最高价氧化物的结构和性质确定晶体类型.
解答 解:该元素的最高正价和最低负价的绝对值相等,根据元素的最高正价和最低负价的绝对值之和等于8,可知该元素最高正价为+4价,最低负价为-4价,
如用X表示该元素符号,x表示该元素的相对原子质量,则其最高价氧化物和其气态氢化物的化学式可分别表示为XO2、XH4,式量之比(x+32):(x+4)=11:4,
解得x=12,该元素为C,碳元素的最高价氧化物形成的晶体为干冰,属于分子晶体,
故选A.
点评 本题考查了元素周期律和晶体的结构,难度中等,具有较强的综合性,掌握元素的最高正价和最低负价的绝对值之和等于8是解题的关键.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
18.糖类是由C、H、O三种元素组成的一类有机化合物.最重要、最简单的单糖是葡萄糖,葡萄糖具有还原性(填还原或者氧化),能和银氨溶液反应产生银镜;淀粉和纤维素都是重要的多糖,它们最终水解产物是葡萄糖.
3.下列各组物质中属于纯净物的是( )
| A. | 氨水 | B. | 氢氧化铁胶体 | C. | 混有冰的水 | D. | 石灰石 |
13.醛可发生分子间的反应,生成烃基醛,如
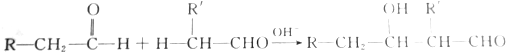
现在用甲醛和乙醛来制备季戊四醇[C(CH2OH)4],消耗的甲醛与乙醛的物质的量之比为( )
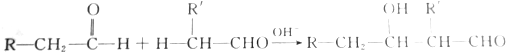
现在用甲醛和乙醛来制备季戊四醇[C(CH2OH)4],消耗的甲醛与乙醛的物质的量之比为( )
| A. | 3:1 | B. | 2:1 | C. | 4:1 | D. | 1:1 |
20.下列说法或表示方法中正确的是( )
| A. | 相同条件下,等质量的硫蒸气和硫固体分别完全燃烧,反应的热效应△H1>△H2 | |
| B. | 由C(石墨)→C(金刚石)△H=+1.9kJ/mol,可知金刚石比石墨稳定 | |
| C. | 已知在101KPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量.则有关氢气燃烧热的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=+285.8kJ/mol | |
| D. | 在稀溶液中,H+ (aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若将含0.5 mol硫酸的浓硫酸与含1 molNaOH的溶液混合,放出的热量大于57.3 kJ |