题目内容
20.下列有关说法正确的是( )| A. | 常温下,pH=8的碱性溶液中不可能存在H2CO3分子 | |
| B. | 常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同 | |
| C. | 0.1mol/LCH3COOH溶液加水稀释,溶液的pH和CH3COOH的电离度均增大 | |
| D. | 将BaCl2溶液滴入含酚酞的Na2CO3溶液,红色褪去,说明BaCl2溶液显酸性 |
分析 A.碳酸钠、碳酸氢钠溶液中都存在碳酸分子;
B.盐酸抑制了水的电离,铵根离子水解促进了水的电离;
C.醋酸稀释后醋酸的电离程度增大,而溶液中氢离子浓度减小;
D.氯化钡溶液为中性溶液,不显示酸性.
解答 解:A.碳酸钠、碳酸氢钠溶液呈碱性,其pH可以为8,两溶液中都存在碳酸分子,故A错误;
B.pH=5的盐酸中氢离子抑制了水的电离,盐酸中氢氧根离子是水电离的,而氯化铵溶液中铵根离子促进了水的电离,溶液中氢离子是水电离的,两溶液中水的电离程度不相同,故B错误;
C.0.1mol/LCH3COOH溶液加水稀释,醋酸的浓度越小,电离程度越大,但是稀释后氢离子浓度减小,所以溶液的pH和CH3COOH的电离度均增大,故C正确;
D.将BaCl2溶液滴入含酚酞的Na2CO3溶液,由于钡离子与碳酸根离子反应生成碳酸钡沉淀,导致碳酸根离子减少之至完全反应,所以溶液红色褪去,而BaCl2溶液显中性,故D错误;
故选C.
点评 本题考查了盐的水解原理及其应用、弱电解质的电离等知识,题目难度中等,明确影响弱电解质电离、盐的水解原理的因素为解答关键,A为易错点,注意碳酸钠、碳酸氢钠溶液中都含有碳酸分子,试题培养了学生的灵活应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.铜锌原电池(如图)工作时,下列叙述不正确的是( )
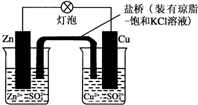

| A. | 负极反应为:Zn-2e-═Zn2+ | B. | 电池反应为:Zn+Cu2+═Zn2++Cu | ||
| C. | 在外电路中,电子从负极流向正极 | D. | 盐桥中的K+移向ZnSO4溶液 |
11.下列热化学方程式正确的是(△H的绝对值均正确)( )
| A. | 表示H2燃烧热:2H2(g)+O2(g)═2H2O1)△H=-571.6 kJ/mol | |
| B. | 表示中和热:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(1)△H=+57.3 kJ/mol | |
| C. | 表示反应热:4Al(s)+3O2(g)═2Al2O3(S)△H=-3352kJ/mol | |
| D. | 表示石墨比金刚石稳定:C(石墨)=C(金刚石)△H=-1.9 kJ/mol |
15.设NA为阿伏加罗常数的值,下列说法正确的是( )
| A. | 3.1g由白磷和红磷组成的混合物中含有磷原子的数目为0.1NA | |
| B. | 0.1mol丙烯醛中含有双键的数目为0.1NA | |
| C. | 标准状况下,2.24L乙醇中含有的分子数目为0.1NA | |
| D. | 0.1mol的氯气全部溶于水后转移电子的数目为0.1NA |
12.以CO(g)和H2(g)为原料合成甲醇反应及其能量变化如图所示,下列判断错误的是( )
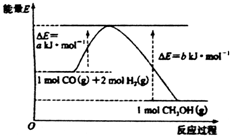

| A. | 该反应的活化能为a kJ•mol-1 | |
| B. | 1mol CO(g)和2 mol H2(g)的能量和大于1mol CH3OH(g)的能量 | |
| C. | 该反应的热化学方程式为:CO(g)+2H2(g)=CH3OH(g)△H=(a-b)kJ•mol-1 | |
| D. | CO(g)+2H2(g)=CH3OH(1)△H=c kJ•mol-1c>(a-b) |
9.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 1 mol FeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA | |
| C. | 2 L 0.5 mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| D. | 1 mol Na2O2固体中含离子总数为4NA |
10.下列各组离子在溶液中能大量共存,加入OH-有沉淀析出,加入H+能放出气体的是( )
| A. | Na+、C1-、NO3-、H+ | B. | K+、Cl-、SO42-、H | ||
| C. | Fe3+、C1-、SO42-、NH4+ | D. | Ca2+、HCO3-、Cl-、NO3- |
