题目内容
3.下列各组离子,能在指定溶液中大量共存的是( )| A. | 无色溶液中:Na+、MnO4-、CO32-、Cl- | |
| B. | 能使紫色石蕊试剂变红的溶液中:OH-、K+、Ba2+、Na+ | |
| C. | 透明的酸性溶液中:Fe3+、Mg2+、Cl-、NO3- | |
| D. | pH=1的溶液中:NH4+、Fe2+、Cl-、NO3- |
分析 A.MnO4-有颜色;
B.能使紫色石蕊试剂变红的溶液呈酸性;
C.离子之间不发生任何反应;
D.pH=1的溶液呈酸性.
解答 解:A.MnO4-有颜色,与题目不符,故A错误;
B.能使紫色石蕊试剂变红的溶液呈酸性,酸性条件下OH-不能大量共存,故B错误;
C.透明的酸性溶液中离子之间不发生任何反应,故C正确;
D.pH=1的溶液呈酸性,酸性条件下Fe2+、NO3-发生氧化还原反应而不能大量共存,故D错误.
故选C.
点评 本题考查离子共存问题,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
13.工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气.对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用.
Ⅰ.脱硝:已知:H2的热值为142.9KJ•g-1
N2(g)+2O2(g)=2NO2(g)△H=+133kJ•mol-1
H2O(g)=H2O(l)△H=-44kJ•mol-1
催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJ•mol-1.
Ⅱ.脱碳:向2L密闭容器中加入2mol CO2、6mol H2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)?CH3OH(l)+H2O(l)
(1)①该反应自发进行的条件是低温(填“低温”、“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是de.
a、混合气体的平均式量保持不变 b、CO2和H2的体积分数保持不变
c、CO2和H2的转化率相等 d、混合气体的密度保持不变
e、1mol CO2生成的同时有3mol H-H键断裂
③CO2的浓度随时间(0~t2)变化如图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6CO2的浓度随时间的变化.

(2)改变温度,使反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0 中的所有物质都为气态.起始温度体积相同(T1℃、2L密闭容器).反应过程中部分数据见表:
①达到平衡时,反应I、II对比:平衡常数K(I)<K(II)(填“>”、“<”或“=”下同);平衡时CH3OH的浓度c(I)<c(II).
②对反应I,前10min内的平均反应速率v(CH3OH)=0.025mol•L-1•min-1,在其它条件不变下,若30min时只改变温度为T2℃,此时H2的物质的量为3.2mol,则T1<T2(填“>”、“<”或“=”).
若30min时只向容器中再充入1mol CO2(g)和1mol H2O(g),则平衡不移动(填“正向”、“逆向”或“不”).
Ⅰ.脱硝:已知:H2的热值为142.9KJ•g-1
N2(g)+2O2(g)=2NO2(g)△H=+133kJ•mol-1
H2O(g)=H2O(l)△H=-44kJ•mol-1
催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJ•mol-1.
Ⅱ.脱碳:向2L密闭容器中加入2mol CO2、6mol H2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)?CH3OH(l)+H2O(l)
(1)①该反应自发进行的条件是低温(填“低温”、“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是de.
a、混合气体的平均式量保持不变 b、CO2和H2的体积分数保持不变
c、CO2和H2的转化率相等 d、混合气体的密度保持不变
e、1mol CO2生成的同时有3mol H-H键断裂
③CO2的浓度随时间(0~t2)变化如图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6CO2的浓度随时间的变化.

(2)改变温度,使反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0 中的所有物质都为气态.起始温度体积相同(T1℃、2L密闭容器).反应过程中部分数据见表:
| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应I 恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应II 绝热恒容 | 0min | 0 | 0 | 2 | 2 |
②对反应I,前10min内的平均反应速率v(CH3OH)=0.025mol•L-1•min-1,在其它条件不变下,若30min时只改变温度为T2℃,此时H2的物质的量为3.2mol,则T1<T2(填“>”、“<”或“=”).
若30min时只向容器中再充入1mol CO2(g)和1mol H2O(g),则平衡不移动(填“正向”、“逆向”或“不”).
14.下列物质中,摩尔质量最大的是( )
| A. | 10mL H2O | B. | 0.8mol H2SO4 | C. | 54g Al | D. | 1gCaCO3 |
11.下列热化学方程式正确的是(△H的绝对值均正确)( )
| A. | 表示H2燃烧热:2H2(g)+O2(g)═2H2O1)△H=-571.6 kJ/mol | |
| B. | 表示中和热:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(1)△H=+57.3 kJ/mol | |
| C. | 表示反应热:4Al(s)+3O2(g)═2Al2O3(S)△H=-3352kJ/mol | |
| D. | 表示石墨比金刚石稳定:C(石墨)=C(金刚石)△H=-1.9 kJ/mol |
15.设NA为阿伏加罗常数的值,下列说法正确的是( )
| A. | 3.1g由白磷和红磷组成的混合物中含有磷原子的数目为0.1NA | |
| B. | 0.1mol丙烯醛中含有双键的数目为0.1NA | |
| C. | 标准状况下,2.24L乙醇中含有的分子数目为0.1NA | |
| D. | 0.1mol的氯气全部溶于水后转移电子的数目为0.1NA |
12.以CO(g)和H2(g)为原料合成甲醇反应及其能量变化如图所示,下列判断错误的是( )
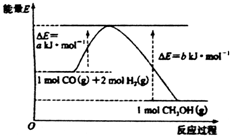

| A. | 该反应的活化能为a kJ•mol-1 | |
| B. | 1mol CO(g)和2 mol H2(g)的能量和大于1mol CH3OH(g)的能量 | |
| C. | 该反应的热化学方程式为:CO(g)+2H2(g)=CH3OH(g)△H=(a-b)kJ•mol-1 | |
| D. | CO(g)+2H2(g)=CH3OH(1)△H=c kJ•mol-1c>(a-b) |
13.有一支25mL酸式滴定管,其中所盛溶液液面恰好在5mL处.现将管内溶液全部排出并用量筒量得该溶液的体积为( )
| A. | 5mL | B. | 20mL | C. | >20mL | D. | <20mL |
