题目内容
13. 常温下,HNO2的电离平衡常数为K=4.6×10-4(已知$\sqrt{4.6}$=2.14),向20mL0.01mol•L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
常温下,HNO2的电离平衡常数为K=4.6×10-4(已知$\sqrt{4.6}$=2.14),向20mL0.01mol•L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )| A. | HNO2的电离方程式为HNO2=NO2-+H+ | |
| B. | a点H2O电离出的c(H+)=2.14×10-3mol•L-1 | |
| C. | b点溶液中离子浓度大小关系为c(NO2-)>c(Na+)>c(H+)>c(OH-) | |
| D. | X值等于20 |
分析 A.亚硝酸为弱酸存在电离平衡,电离方程式用可逆号;
B.由HNO2?H++NO2-,K=$\frac{c({H}^{+})c(N{{O}_{2}}^{-})}{c(HN{O}_{2})}$≈$\frac{{c}^{2}({H}^{+})}{c(HN{O}_{2})}$,4.6×10-4≈$\frac{{c}^{2}({H}^{+})}{0.01}$,得到c(H+)=2.14×10-3mol/L;
C.b点溶液为HNO2、NaNO2混合溶液,且浓度比为1:1;由NO2-+H2O?HNO2+OH-,HNO2?H++NO2-,电离程度大于水解程度,可知溶液呈酸性;
D.向20mL0.01mol•L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,若恰好反应需要氢氧化钠溶液体积20,ml,C点是溶液呈中性,溶质为HNO2、NaNO2混合溶液.
解答 解:A.HNO2的电离平衡常数为K=4.6×10-4,亚硝酸为弱酸存在电离平衡,电离方程式为HNO2?NO2-+H+,故A错误;
B.由HNO2?H++NO2-,K=$\frac{c({H}^{+})c(N{{O}_{2}}^{-})}{c(HN{O}_{2})}$≈$\frac{{c}^{2}({H}^{+})}{c(HN{O}_{2})}$,4.6×10-4≈$\frac{{c}^{2}({H}^{+})}{0.01}$,得到c(H+)=2.14×10-3mol/L,水电离出氢离子浓度远小于酸电离出氢离子,故B错误;
C.b点溶液为HNO2、NaNO2混合溶液,且浓度比为1:1;由NO2-+H2O?HNO2+OH-,HNO2?H++NO2-,电离程度大于水解程度,可知溶液呈酸性,离子浓度大小为c(NO2-)>c(Na+)>c(H+)>c(OH-),故C正确;
D.向20mL0.01mol•L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,若恰好反应需要氢氧化钠溶液体积20,ml,C点是溶液呈中性,溶质为HNO2、NaNO2混合溶液,X<20ml,故D错误;
故选C.
点评 本题考查了弱电解质电离平衡、离子浓度大小比较、平衡常数计算、图象变化分析判断,注意中性溶液中溶质的判断,题目难度中等.

| A. | H2S沸点比H2O高 | B. | NH3和CO2均属于弱电解质 | ||
| C. | NH3(l)气化为NH3(g)放出热量 | D. | HCOOH能与NH4HCO3反应放出CO2 |
| A. | 糖类、油脂、蛋白质都是高分子化合物 | |
| B. | 淀粉遇碘溶液变蓝 | |
| C. | 正丁烷和异丁烷互为同分异构体 | |
| D. | 天然气的主要成分是甲烷 |
| A. | 油脂、纤维素和蛋白质均能发生水解,且最终水解产物均不相同 | |
| B. | 酒精浓度过高或过低都不利于杀菌消毒,医用酒精中乙醇的质量分数为75% | |
| C. | 鸡蛋清和淀粉溶液都属于胶体,遇到硫酸铜溶液可以发生胶体聚沉 | |
| D. | 纤维素可以加强肠胃蠕动,有助于消化,因此纤维素是人体的营养物质 |
| A. | 金刚石和C60 | B. | 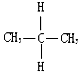 与 与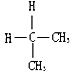 | ||
| C. | 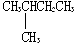 与 与 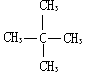 | D. | CH3CH3与CH3CH2CH2CH3 |
| 化学式 | HA(A代表某种酸根) | HNO2 | H2CO3 |
| Ka | Ka=4.9×10-10 | Ka=4.6×10-4 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
(1)用离子方程式表示NaNO2溶液呈碱性的原因NO2-+H2O?HNO2+OH-.
(2)NaHCO3的电离方程式是NaHCO3=Na++HCO3-.
(3)A-、CO32-、HCO3-在水中结合H+的能力由大到小的顺序为CO32->A->HCO3->NO2-.
(4)25℃时,等物质的量浓度的HA和NaA的混合溶液呈碱性,则该混合溶液中各离子浓度大小关系为c(Na+)>c(A-)>c(OH-)>c(H+),解释HA和NaA的混合溶液呈碱性的原因A-离子水解程度大于HA电离程度.
(5)写出NaA溶液中通少量CO2的离子方程式A-+CO2+H2O=HA+HCO3-.
(6)某同学用Na2CO3和NaHCO3溶液进行如图所示实验.
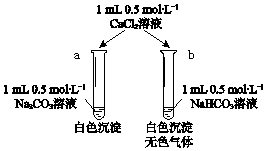
①充分反应后a试管中大量存在的离子是Na+、Cl-.
②用离子方程式表示b试管中发生的反应2HCO3-+Ca2+=CaCO3↓+CO2↑+H2O.
| A. | 甲烷的燃烧 | B. | 浓硫酸的稀释 | ||
| C. | NH4Cl与Ba(OH)2•8H2O反应 | D. | 铝热反应 |
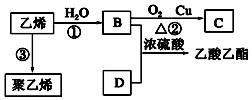 已知乙烯能发生以下转化:
已知乙烯能发生以下转化: ,列举聚乙烯的一种用途制塑料.
,列举聚乙烯的一种用途制塑料.