题目内容
4.波士顿大学的研究学者用HCOOH、H2S、NH3、CO2、H2O、NH4HCO3、N2等物质,借助计算机模拟原始的新陈代谢,以支持“现代生物源自矿物地球化学”这一观点.下列说法正确的是( )| A. | H2S沸点比H2O高 | B. | NH3和CO2均属于弱电解质 | ||
| C. | NH3(l)气化为NH3(g)放出热量 | D. | HCOOH能与NH4HCO3反应放出CO2 |
分析 A.水分子间存在氢键,沸点较高;
B.NH3和CO2在水溶液中本身不能发生电离;
C.液体变为气体,应吸收能量;
D.甲酸的酸性比碳酸强.
解答 解:A.由于O的非金属性较强,水分子间存在氢键,分子间作用力较强,则沸点较高,故A错误;
B.NH3和CO2在水溶液中与水反应生成可电离的物质,但本身不能发生电离,属于非电解质,故B错误;
C.气体的能量较高,液体变为气体,应吸收能量,故C错误;
D.甲酸的酸性比碳酸强,则HCOOH能与NH4HCO3反应放出CO2,符合以强制弱的规律,故D正确.
故选D.
点评 本题考查较为综合,涉及氢键、电解质、化学反应与能量变化以及物质的性质等知识,为高频考点,侧重考查学生的分析能力,注意把握相关物质的性质,难度不大.

练习册系列答案
相关题目
2.下列有机反应属于同一反应类型的是( )
| A. | 甲烷制一氯甲烷、苯制溴苯 | |
| B. | 乙醇制乙醛、乙醇和乙酸制乙酸乙酯 | |
| C. | 乙醇制乙烯、乙烯制乙醇 | |
| D. | 苯制环己烷、乙酸乙酯水解 |
15.如图所示为反应2H2(g)+O2(g)═2H2O(g)的能量变化示意图.下列说法正确的是( )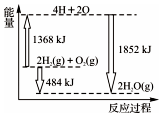

| A. | H2(g)和O2(g)反应生成H2O(g),这是个吸热过程 | |
| B. | 由2 mol H2和1 mol O2变成4 mol H、2 mol O原子,这是个放热过程 | |
| C. | 2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),共放出484 KJ能量 | |
| D. | 4 mol H、2 mol O生成2 mol H2O(g),共放出484 KJ能量 |
19.烯烃被酸性高锰酸钾溶液氧化的规律是,双键两端的基团=CH2变成CO2,=CHR变成RCOOH,
 变成
变成 ,现有某溴代烷A,分子式为C4H9Br,在NaOH醇溶液中加热得到有机物B,B被酸性高锰酸钾溶液氧化后不可能得到的产物是( )
,现有某溴代烷A,分子式为C4H9Br,在NaOH醇溶液中加热得到有机物B,B被酸性高锰酸钾溶液氧化后不可能得到的产物是( )
 变成
变成 ,现有某溴代烷A,分子式为C4H9Br,在NaOH醇溶液中加热得到有机物B,B被酸性高锰酸钾溶液氧化后不可能得到的产物是( )
,现有某溴代烷A,分子式为C4H9Br,在NaOH醇溶液中加热得到有机物B,B被酸性高锰酸钾溶液氧化后不可能得到的产物是( )| A. | 只有CH3COOH | B. | CO2和 CH3COCH3 | ||
| C. | CO2和CH3CH2COOH | D. | HCOOH和CH3CH2COOH |
9.某同主族(或同周期)元素的主要化合价的变化规律如图所示,它们可能位于周期表( )


| A. | ⅠA族 | B. | ⅡA族 | C. | 第二周期 | D. | 第三周期 |
16.据探测月球土壤中吸附着数百万吨可作为核聚变材料的${\;}_{2}^{3}$He.下列有关${\;}_{2}^{3}$He的说法正确的是( )
| A. | 质量数为2 | B. | 质子数为2 | C. | 质子数为3 | D. | 质量数为1 |
13.可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是( )
| A. | 将混合气体通过盛有硫酸的洗气瓶 | |
| B. | 将混合气体通过盛有水的洗气瓶 | |
| C. | 将混合气体通过盛有足量溴水的洗气瓶 | |
| D. | 将混合气体通过盛有澄清石灰水的洗气瓶 |
13. 常温下,HNO2的电离平衡常数为K=4.6×10-4(已知$\sqrt{4.6}$=2.14),向20mL0.01mol•L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
常温下,HNO2的电离平衡常数为K=4.6×10-4(已知$\sqrt{4.6}$=2.14),向20mL0.01mol•L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
 常温下,HNO2的电离平衡常数为K=4.6×10-4(已知$\sqrt{4.6}$=2.14),向20mL0.01mol•L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
常温下,HNO2的电离平衡常数为K=4.6×10-4(已知$\sqrt{4.6}$=2.14),向20mL0.01mol•L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )| A. | HNO2的电离方程式为HNO2=NO2-+H+ | |
| B. | a点H2O电离出的c(H+)=2.14×10-3mol•L-1 | |
| C. | b点溶液中离子浓度大小关系为c(NO2-)>c(Na+)>c(H+)>c(OH-) | |
| D. | X值等于20 |
