题目内容
5.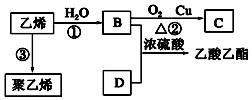 已知乙烯能发生以下转化:
已知乙烯能发生以下转化:(1)C中含官能团名称醛基;
(2)写出B与D反应的化学方程式CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;反应类型:酯化反应或取代反应.
(3)写出反应③的化学方程式:
 ,列举聚乙烯的一种用途制塑料.
,列举聚乙烯的一种用途制塑料.
分析 乙烯与水发生加成反应生成B,则B为CH3CH2OH,乙醇在Cu作催化剂条件下发生氧化反应CH3CHO,C为CH3CHO,B与D反应生成乙酸乙酯(CH3COOCH2CH3),则D为CH3COOH,乙烯发生加聚反应生成聚乙烯(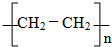 ),以此来解答
),以此来解答
解答 解:(1)C为CH3CHO,含有的官能团为醛基,故答案为:醛基;
(2)B与D反应生成乙酸乙酯(CH3COOCH2CH3),方程式为CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,为酯化反应或取代反应,
故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O; 酯化反应或取代反应;
(3)乙烯发生加聚反应得到聚乙烯,即 ,聚乙烯可用于制塑料,
,聚乙烯可用于制塑料,
故答案为: ;制塑料.
;制塑料.
点评 本题考查有机物的推断,为高频考点,把握有机物的性质、转化反应中官能团的变化、有机反应等为解答的关键,侧重分析与推断能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13. 常温下,HNO2的电离平衡常数为K=4.6×10-4(已知$\sqrt{4.6}$=2.14),向20mL0.01mol•L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
常温下,HNO2的电离平衡常数为K=4.6×10-4(已知$\sqrt{4.6}$=2.14),向20mL0.01mol•L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
 常温下,HNO2的电离平衡常数为K=4.6×10-4(已知$\sqrt{4.6}$=2.14),向20mL0.01mol•L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
常温下,HNO2的电离平衡常数为K=4.6×10-4(已知$\sqrt{4.6}$=2.14),向20mL0.01mol•L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )| A. | HNO2的电离方程式为HNO2=NO2-+H+ | |
| B. | a点H2O电离出的c(H+)=2.14×10-3mol•L-1 | |
| C. | b点溶液中离子浓度大小关系为c(NO2-)>c(Na+)>c(H+)>c(OH-) | |
| D. | X值等于20 |
16.下列化合物既能与稀盐酸反应又能与NaOH溶液反应的是( )
①Al
②(NH4)2CO3
③Al2O3
④Ca(HCO3)2
⑤AgNO3
⑥Al(OH)3.
①Al
②(NH4)2CO3
③Al2O3
④Ca(HCO3)2
⑤AgNO3
⑥Al(OH)3.
| A. | ①②③④⑤⑥ | B. | ②③④⑥ | C. | ②③④⑤⑥ | D. | ①②③⑥ |
13.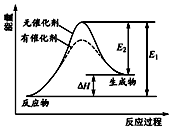 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A. | 加入催化剂,减小了反应的热效应 | |
| B. | 催化剂能降低反应的活化能 | |
| C. | 该反应的△H=E2-E1 | |
| D. | 该图可以表示燃料燃烧反应的能量变化 |
20.X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若Y原子的最外层电子数是次外层电子数的3倍.下列说法错误的是( )
| X | Y | ||
| Z | W |
| A. | 气态氢化物的热稳定性:X<Y | |
| B. | 最高价氧化物对应水化物的酸性:W>Z>X | |
| C. | X、Y元素均存在同素异形体 | |
| D. | W的单质具有漂白性,能使干燥的有色布条褪色 |
10.根据元素周期律的知识,下列两者性质比较中,不正确的是( )
| A. | 热稳定性:PH3<NH3 | B. | 金属性强弱:Na>Mg>Al | ||
| C. | 酸性强弱:HF>HCl>HBr>HI | D. | 原子半径:K>Si>Cl>F |
1.下列措施或事实不能用勒沙特列原理解释的是( )
| A. | H2、I2(g)、HI平衡混合气体加压后颜色变深(已知:H2+I2?2HI) | |
| B. | 棕红色的NO2加压后颜色先变深后变浅(已知:2NO2 (g)?N2O4 (g)) | |
| C. | 工业上生产硫酸的过程中,使用过量的空气以提高SO2的利用率 | |
| D. | 滴加酚酞的氨水中加入氯化铵固体后红色变浅 |
18.某元素最高价含氧酸的化学式是H2RO4,则该元素的气态氢化物化学式可表示为( )
| A. | HR | B. | H2R | C. | RH4 | D. | 不确定 |
19.为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法都正确的是( )
| 序号 | 不纯物 | 除杂试剂 | 分离方法 |
| A | CH4(C2H4) | 酸性KMnO4溶液 | 洗气 |
| B | 苯(Br2) | NaOH溶液 | 过滤 |
| C | C2H5OH(H2O) | 新制生石灰 | 蒸馏 |
| D | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |