题目内容
2.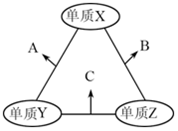 X、Y、Z是原子序数依次增大的三种短周期元素,三种元素的原子序数之和为35,且Z的原子序数是X的原子序数的2倍.X、Y、Z三种元素的常见单质在适当条件下可发生如图所示变化,下列说法不正确的是( )
X、Y、Z是原子序数依次增大的三种短周期元素,三种元素的原子序数之和为35,且Z的原子序数是X的原子序数的2倍.X、Y、Z三种元素的常见单质在适当条件下可发生如图所示变化,下列说法不正确的是( )| A. | 元素X,Z的单质均存在同素异形体 | B. | A和C溶于水,溶液均显碱性 | ||
| C. | A和B都可能具有漂白性 | D. | Z的氧化物的水化物一定是强酸 |
分析 Z的原子序数是X的原子序数的2倍,如X为O,则Z为S元素,三种元素的原子序数之和为35,则Y为Na,由转化关系可知A为Na2O或Na2O2,B为SO2,C为Na2S,结合对应物质的性质解答该题.
解答 解:由以上分析可知X为O、Y为Na、Z为S,A为Na2O或Na2O2,B为SO2,C为Na2S,
A.X为O、Z为S,都存在多种同素异形体,如氧气、臭氧、斜方硫、单斜硫等,故A正确;
B.A为Na2O或Na2O2,与水反应生成氢氧化钠,Na2S为强碱弱酸盐,溶液都成碱性,故B正确;
C.A如为Na2O2,具有漂白性,B为SO2,也具有漂白性,故C正确;
D.Z为S,对应的氧化物如为SO2,则对应的酸为弱酸,故D错误.
故选D.
点评 本题考查无机物的推断,为高频考点,侧重考查学生的分析能力,注意把握原子的结构与元素周期律,把握物质的性质以及转化关系,难度不大.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
13.下列说法正确的是( )
| A. | 加入过量氨水,有白色沉淀生成,则原溶液中一定有Al3+ | |
| B. | 加入盐酸酸化的BaCl2溶液,有白色沉淀生成,则原溶液一定有SO42- | |
| C. | 向某溶液中先加入氯水振荡,再加KSCN溶液后显血红色,该溶液中一定有Fe2+ | |
| D. | 向某溶液中先加入新制饱和氯水,再加CCl4,振荡,分层,下层呈橙红色,则该溶液中一定含有Br- |
10.4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性.
回答下列问题:
(1)元素x在周期表中的位置是第三周期第ⅡA族,其单质可采用电解熔融MgCl2的方法制备.
(2)气体分子(mn)2的电子式为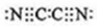 ,(mn)2称为拟卤素,性质与卤素相似,其与氢氧化钠溶液反应的化学方程式为2NaOH+(CN)2=NaCN+NaOCN+H2O.
,(mn)2称为拟卤素,性质与卤素相似,其与氢氧化钠溶液反应的化学方程式为2NaOH+(CN)2=NaCN+NaOCN+H2O.
(3)已知氰化钠(NaCN),可以与很多金属形成络合物,因此工业上采用氰化法提炼金:用稀的氰化钠溶液处理粉碎了的金矿石,通入空气,使金矿石中的金粒溶解,生成能溶于水的络合物Na[Au(CN)2],其反应方程式为:①4Au+8NaCN+2H2O+O2═4Na[Au(CN)2]+4NaOH,Na[Au(CN)2]在水溶液中的电离方程式为:②Na[Au(CN)2]═Na++[Au(CN)2]-
然后再用锌从溶液中把金置换出来,锌转化为Na2[Zn(CN)4].据此,请利用①写出在空气中用氰化钠溶液提取金的电极反应式:正极:O2+2H2O+4e-═4OH-,负极:Au+2CN--e-═[Au(CN)2]-.
(4)若人不慎氰化钠中毒,可用Na2S2O3缓解,二者反应得到两种含硫元素的离子,其中一种遇到Fe3+可变为红色.写出解毒原理的相关离子方程式S2O32-+CN-═SCN-+SO32-.
| m | n | ||
| x | y |
(1)元素x在周期表中的位置是第三周期第ⅡA族,其单质可采用电解熔融MgCl2的方法制备.
(2)气体分子(mn)2的电子式为
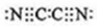 ,(mn)2称为拟卤素,性质与卤素相似,其与氢氧化钠溶液反应的化学方程式为2NaOH+(CN)2=NaCN+NaOCN+H2O.
,(mn)2称为拟卤素,性质与卤素相似,其与氢氧化钠溶液反应的化学方程式为2NaOH+(CN)2=NaCN+NaOCN+H2O.(3)已知氰化钠(NaCN),可以与很多金属形成络合物,因此工业上采用氰化法提炼金:用稀的氰化钠溶液处理粉碎了的金矿石,通入空气,使金矿石中的金粒溶解,生成能溶于水的络合物Na[Au(CN)2],其反应方程式为:①4Au+8NaCN+2H2O+O2═4Na[Au(CN)2]+4NaOH,Na[Au(CN)2]在水溶液中的电离方程式为:②Na[Au(CN)2]═Na++[Au(CN)2]-
然后再用锌从溶液中把金置换出来,锌转化为Na2[Zn(CN)4].据此,请利用①写出在空气中用氰化钠溶液提取金的电极反应式:正极:O2+2H2O+4e-═4OH-,负极:Au+2CN--e-═[Au(CN)2]-.
(4)若人不慎氰化钠中毒,可用Na2S2O3缓解,二者反应得到两种含硫元素的离子,其中一种遇到Fe3+可变为红色.写出解毒原理的相关离子方程式S2O32-+CN-═SCN-+SO32-.
17.下列分子中,所有原子都处在同一平面的是( )
| A. | 环己烯 | B. | 丙烯 | C. | 乙烷 | D. | 氯乙烯 |
11.现有部分短周期元素的性质或原子结构如表:
(1)元素T在周期表中的位置是三周期ⅥA族.
(2)元素X的一种同位素可测定文物年代,这种同位素的符号是14C.
(3)元素Y与氢元素形成一种分子YH3,写出该粒子的化学式:NH3.
(4)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b.
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(5)T、X、Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是HClO4>H2SO4>H2CO3(用化学式表示).
| 元素编号 | 元素性质或原子结构 |
| T | M层上的电子数是原子核外电子层数的2倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(2)元素X的一种同位素可测定文物年代,这种同位素的符号是14C.
(3)元素Y与氢元素形成一种分子YH3,写出该粒子的化学式:NH3.
(4)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b.
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(5)T、X、Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是HClO4>H2SO4>H2CO3(用化学式表示).
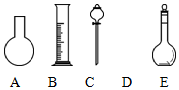 实验室需要0.80mol•L-1 NaOH溶液475mL和0.40mol•L-1硫酸500mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.80mol•L-1 NaOH溶液475mL和0.40mol•L-1硫酸500mL.根据这两种溶液的配制情况回答下列问题: