题目内容
10.Cr位于元素周期表第4周期第ⅥB族,其原子核外电子排布式为[Ar]3d54s1.分析 铬的原子序数为24,位于周期表第4周期ⅥB族,根据能量最低原则、泡利不相容原理和洪特规则综合考虑,写出核外电子排布式.
解答 解:铬的原子序数为24,位于周期表第4周期ⅥB族,原子核外电子数为24,3d能级上的原子轨道处于半满时,能量较低,因此核外电子排布式为[Ar]3d54s1,故答案为:4;ⅥB;[Ar]3d54s1.
点评 本题考查了原子结构、原子核外电子排布等知识点,根据构造原理书写其电子排布式,明确元素周期律的内容,难度不大.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
20.把Ba(OH)2溶液滴入明矾(KAl(SO4)2•12H2O)溶液中,使SO42-全部转化成BaSO4沉淀,此时铝元素的主要存在形式是( )
| A. | Al3+ | B. | Al(OH)3 | C. | [Al(OH)4]- | D. | Al3+和Al(OH)3 |
18.下列物质的命名错误的是( )
| A. | 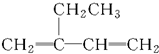 2-乙基-1,3-丁二烯 2-乙基-1,3-丁二烯 | B. | CH2=CH-CH2-CH3 1-丁烯 | ||
| C. | 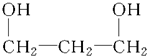 1,3-二丙醇 1,3-二丙醇 | D. | 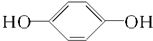 1,4-苯二酚 1,4-苯二酚 |
5.某氯原子的质量是a g,12C原子的质量是bg,用NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 氯元素的相对原子质量为$\frac{12b}{a}$ | |
| B. | mg该氯原子的物质的量一定是$\frac{m}{(a{N}_{A})}$mol | |
| C. | 该氯元素的摩尔质量是aNA | |
| D. | ng该氯原子所含的电子数为$\frac{n}{a}$ |
15.下列分子或离子中,VSEPR模型名称与分子或离子的立体构型名称不一致的是( )
| A. | CO2 | B. | H2O | C. | CO32- | D. | CCl4 |
19.某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释的pH变化曲线如图所示,下列判断正确的是( )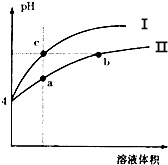

| A. | Ⅰ为氯化铵溶液稀释时pH值变化曲线 | |
| B. | b点比c点溶液的导电能力强 | |
| C. | a点溶液中c(H+)+c(NH3•H2O)=c(OH-) | |
| D. | b点比a点溶液中的水的电离程度大,但两点的KW相同 |
9.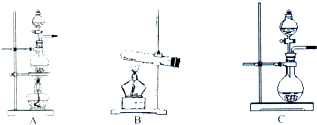 如表是实验室制备气体的有关内容:
如表是实验室制备气体的有关内容:
(1)上述气体中,从反应中有无电子转移的角度看,明显不同于其他气体的是NH3,写出实验室制取该气体的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(2)根据表中所列实验原理,从如图装置中选择合适的发生装置,将其编号填入上表的空格中.
(3)若用上述制备O2的装置制备NH3,应选择的试剂为浓氨水和氢氧化钠(或生石灰等).
(4)在浓CaCl2溶液中通人NH3和CO2可以制得纳米级碳酸钙,制取时应先通入的气体是NH3,制取纳米级碳酸钙的化学方程式为CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl.试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级取少量样品和水混合形成分散系,用一束光从侧面照射,若出现光亮的通路,则证明样品是纳米级,否则不是.
(5)制备Cl2需用8mol•L-1的盐酸100mL,现用12mol•L-1的盐酸来配制.
①需要用量筒量取12mol•L-1的盐酸的体积为66.7mL;
②实验室提供有如下仪器,为完成配制需要选择的仪器为(填序号)ACFGH.
A.100mL量筒B.托盘天平C.玻璃棒D.50mL容量瓶
E.10mL量筒F.胶头滴管G.100mL烧杯H.100mL容量瓶
③下列实验操作中.不正确的是BC(填写标号).
A.使用容量瓶前,检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,用量筒量取浓盐酸并沿玻璃棒倒入容量瓶中,缓慢加人蒸馏水到距离刻度线1~2cm处,改用胶头滴管滴加蒸馏水直到凹液面的最低点和刻度线相平
D.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转和摇动多次.
 如表是实验室制备气体的有关内容:
如表是实验室制备气体的有关内容:| 编号 | 实验内容 | 实验原理 | 发生装置 |
| ① | 制氧气 | H2O2→O2 | C |
| ② | 制氨气 | NH4Cl→NH3 | B |
| ③ | 制氯气 | HCl→Cl2 | A或C |
(2)根据表中所列实验原理,从如图装置中选择合适的发生装置,将其编号填入上表的空格中.
(3)若用上述制备O2的装置制备NH3,应选择的试剂为浓氨水和氢氧化钠(或生石灰等).
(4)在浓CaCl2溶液中通人NH3和CO2可以制得纳米级碳酸钙,制取时应先通入的气体是NH3,制取纳米级碳酸钙的化学方程式为CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl.试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级取少量样品和水混合形成分散系,用一束光从侧面照射,若出现光亮的通路,则证明样品是纳米级,否则不是.
(5)制备Cl2需用8mol•L-1的盐酸100mL,现用12mol•L-1的盐酸来配制.
①需要用量筒量取12mol•L-1的盐酸的体积为66.7mL;
②实验室提供有如下仪器,为完成配制需要选择的仪器为(填序号)ACFGH.
A.100mL量筒B.托盘天平C.玻璃棒D.50mL容量瓶
E.10mL量筒F.胶头滴管G.100mL烧杯H.100mL容量瓶
③下列实验操作中.不正确的是BC(填写标号).
A.使用容量瓶前,检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,用量筒量取浓盐酸并沿玻璃棒倒入容量瓶中,缓慢加人蒸馏水到距离刻度线1~2cm处,改用胶头滴管滴加蒸馏水直到凹液面的最低点和刻度线相平
D.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转和摇动多次.