题目内容
20.工业上生产Na、Ca、Mg都用电解熔融的氯化物,但K不能用电解熔融态的方法得到,因金属钾易溶于熔融态的KCl而有危险,很难制得K,且降低电流效率.现生产钾是用金属钠和KCl在850℃反应制取,有关的反应式为:KCl+Na=NaCl+K↑下列说法错误的是( )| A. | 该反应850℃的选择是基于熔沸点的考虑 | |
| B. | 该反应不能在空气中进行 | |
| C. | 该反应属于置换反应的类型 | |
| D. | 该反应表明钠比钾的活动性强 |
分析 A.根据平衡移动原理,为使反应向正反应方向进行,可使生成物从平衡体系中分离出来,根据Na和K的沸点大小,制取的适宜温度应能使K蒸汽分离出,而钠为液体;
B、钠与钾是活泼金属极易被空气中的氧气氧化;
C、一种单质和一种化合物反应生成另一种单质和另一种化合物,是置换反应;
D、该反应是因为K的沸点低,不是钠比钾的活动性强.
解答 解:A.K的沸点774℃,Na的沸点882.9℃,制取的适宜温度应能使K蒸汽分离出,而钠为液体,所以选择的温度应在774℃~882.9℃之间,所以850℃的选择是基于熔沸点的考虑,故A正确;
B、钠与钾是活泼金属极易被空气中的氧气氧化,所以反应不能在空气中进行,故B正确;
C.该反应符合置换反应的特点,故C正确;
D.在金属活动顺序表中,K排在Na的前面,K的还原性比Na强,上述反应能够发生是因为K的沸点比Na低,故D错误;
故选D.
点评 本题通过工业用Na制取K的反应,考查了化学平衡的移动、置换反应等基本知识,注意KCl+Na=NaCl+K↑得以发生的原因是因为K的沸点比Na低是解答的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列说法中正确的是( )
| A. | 2 g 氦气所含有的原子数目是0.25 NA | |
| B. | 常温常压下,0.5 mol Cl2所占有的体积约为11.2 L | |
| C. | 标准状况下,0.9 mL水的质量约为0.9 g | |
| D. | 0.5 mol/L Na2SO4 溶液中Na+ 的物质的量是1 mol |
8.下列硫化物中不能直接用金属单质和硫单质反应制得的是( )
| A. | CuS | B. | FeS | C. | ZnS | D. | MgS |
15.下列关于有机物的说法正确的是( )
| A. | 1,3-丁二烯与溴单质加成的产物只有2种 | |
| B. | 酚酞(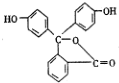 )属于醇 )属于醇 | |
| C. | 可以用溴水将四氯化碳和乙醇鉴别开来 | |
| D. | 分子组成相差一个或若干个CH2原子团的化合物肯定互为同系物 |
5.下列说法正确的是( )
| A. | 冰的晶体中每个水分子可与周围两个水分子形成氢键 | |
| B. | 手性碳原子不一定是饱和碳原子 | |
| C. | 区分晶体与非晶体最科学的方法是X-射线衍射法 | |
| D. | 晶体中有阳离子就一定有阴离子 |
12.某无色气体可能含有甲烷、一氧化碳、氢气中的一种或几种,依次进行下列实验(假设每步反应或吸收均完全):
①无色气体在足量氧气中燃烧;
②燃烧生成的气体通过盛有浓硫酸的洗气瓶,装置增重3.6克;
③再将剩余气体通过盛有澄清石灰水溶液的洗气瓶,装置增重4.4克.下列推断正确的是( )
①无色气体在足量氧气中燃烧;
②燃烧生成的气体通过盛有浓硫酸的洗气瓶,装置增重3.6克;
③再将剩余气体通过盛有澄清石灰水溶液的洗气瓶,装置增重4.4克.下列推断正确的是( )
| A. | 该气体可能只含有一氧化碳、氢气 | B. | 该气体可能只含有甲烷、一氧化碳 | ||
| C. | 该气体一定只含有甲烷 | D. | 该气体一定只含有甲烷、氢气 |
9.常温常压下,取下列四种有机物各1mol,分别在足量的氧气中燃烧,消耗氧气最多的是( )
| A. | C2H5OH | B. | CH4 | C. | C2H4O | D. | C3H8 |
3.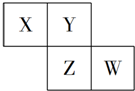 X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )
 X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )| A. | 阴离子的半径从大到小排列顺序为:X>Y>Z>W | |
| B. | X、Y、Z、W元素的氢化物分子间都可以形成氢键 | |
| C. | Y的两种同素异形体在常温下可以相互转化 | |
| D. | 最高价氧化物对应的水化物的酸性:W>Z |