题目内容
18.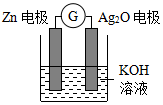 银锌电池是一种常见化学电源,其原理反应:Zn+Ag2O+H2O═Zn(OH)2+2Ag,其工作示意图如图.下列说法不正确的是( )
银锌电池是一种常见化学电源,其原理反应:Zn+Ag2O+H2O═Zn(OH)2+2Ag,其工作示意图如图.下列说法不正确的是( )| A. | Zn电极是负极 | |
| B. | Ag2O电极上发生还原反应 | |
| C. | Zn电极的电极反应式:Zn-2e-+2OH-═Zn(OH)2 | |
| D. | 放电前后电解质溶液的pH保持不变 |
分析 原电池反应Zn+Ag2O+H2O=Zn(OH)2+2Ag中,负极反应为Zn+2OH--2e-=Zn(OH)2、正极反应为Ag2O+H2O+2e-=2Ag+2OH-,电子由负极流向正极,以此来解答.
解答 解:A、活泼金属Zn为负极,故A正确;
B、正极反应为Ag2O+H2O+2e-=2Ag+2OH-,发生还原反应,故B正确;
C、负极反应为Zn+2OH--2e-=Zn(OH)2,故C正确;
D、氢氧根离子物质的量虽然不变,但水的量减少,KOH的浓度增大,pH增大,故D错误;
故选D.
点评 本题考查原电池知识,题目难度不大,明确电极反应、原电池的正负极以及电池反应的关系,注意结合氧化还原反应来分析.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
6.1LNaOH溶液中含有20gNaOH,该溶液物质的量浓度为( )
| A. | 0.5mol/L | B. | 0.05mol/L | C. | 0.4mol/L | D. | 0.01mol/L |
13.下列说法不正确的是( )
| A. | 实验室应将钠保存在煤油中 | |
| B. | 分液漏斗和容量瓶在使用前都要检漏 | |
| C. | 可用酒精代替CCl4萃取碘水中的碘单质 | |
| D. | 金属镁失火不可用水来灭火 |
3.化学与科学技术、生产生活密切相关.下列说法正确的是( )
| A. | “人造太阳”核心组件之一为高纯铍,可通过H2还原BeO制铍 | |
| B. | 富脂食品包装时,放入活性铁粉等抗氧剂,以防止油脂氧化变质 | |
| C. | 煤气化直接制烯烃研究取得重大突破,煤汽化可同时获得焦炭 | |
| D. | 俄罗斯发生了严重的假酒事件,假酒中的甲醇与乙二醇互为同系物 |
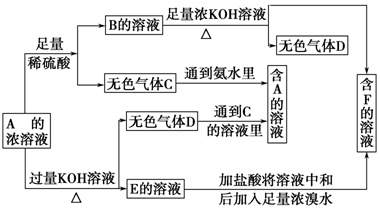
 如图是某次实验探究铁及其化合物性质的流程图:
如图是某次实验探究铁及其化合物性质的流程图: