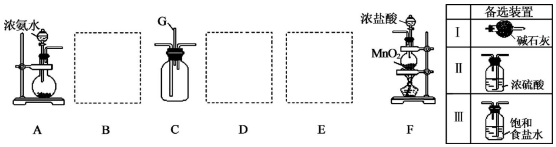
��Ŀ����
2��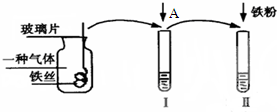 ��ͼ��ij��ʵ��̽�������仯�������ʵ�����ͼ��
��ͼ��ij��ʵ��̽�������仯�������ʵ�����ͼ������ͼʾ���������ʾ�ش��������⣺
��1��ʵ��ʱijͬѧ��ʹ����ƿ�����ɸ����Σ�����ƿ��ӦԤ���ռ�һ�ֻ���ɫ���壬��������Ӧ�Ļ�ѧ����ʽ�ǣ�2Fe+3Cl2=2FeCl3��
��2������Ƽ�ʵ����ȷ��������Ӧ�������˸���ȡ�������壬��ˮ���Ƴ���Һ�������мӼ���KSCN��Һ������Һ��Ѫ��ɫ��˵���и��������ɣ��������������ɣ�
��3��������ƿ�е�������Һ�����Թ�I�У�Ȼ���������ĵ���A�����ã���Һ������ɫ����ʵ��֤�����������Ľ�����������Cu2+����д���ӷ��ţ���
��4�����Թ�I�е�Һ�嵹���Թܢ��У��ټ���������ۣ������ˣ���ʵ�������ʹ�õ��IJ����������ձ���©���⣬���в�������
���� ��1���û���ɫ������Ϊ����������������Ӧ�����Ȼ�����
��2������Ϊ���������ӣ����������軯����Һ���������ӣ�
��3����Һ������ɫ��˵����Ӧ������ͭ���ӣ�
��4������ʱ��Ҫ�õ�����������������
��� �⣺��1��ʵ��ʱijͬѧ��ʹ����ƿ�����ɸ����Σ�����ƿ��ӦԤ���ռ�һ�ֻ���ɫ���壬������Ϊ��������Ӧ�Ļ�ѧ����ʽΪ��2Fe+3Cl2=2FeCl3��
�ʴ�Ϊ��2Fe+3Cl2=2FeCl3��
��2��ȷ��������Ӧ�������˸��������Ƚ������ܽ⣬Ȼ�������軯����Һ���飬��������Ϊ��ȡ�������壬��ˮ���Ƴ���Һ�������мӼ���KSCN��Һ������Һ��Ѫ��ɫ��˵���и��������ɣ��������������ɣ�
�ʴ�Ϊ��ȡ�������壬��ˮ���Ƴ���Һ�������мӼ���KSCN��Һ������Һ��Ѫ��ɫ��˵���и��������ɣ��������������ɣ�
��3��������ƿ�е�������Һ�����Թ�I�У�Ȼ���������ĵ���A�����ã���Һ������ɫ��˵����Ӧ������ͭ���ӣ����ʵ��֤�����������Ľ�����������Cu2+��
�ʴ�Ϊ��Cu2+��
��4����ʵ�����Ϊ���ˣ����˲����õ��IJ����������ձ���©���Ͳ����������Ի�ȱ�ٲ�������
�ʴ�Ϊ����������
���� ���⿼���������仯�������ʣ���Ŀ�Ѷ��еȣ���ȷʵ��Ŀ��Ϊ���ؼ���ע���������ճ���Ԫ�ؼ��仯�������ʣ�����������ѧ���ķ�����������ѧʵ��������

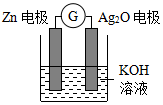 ��п�����һ�ֳ�����ѧ��Դ����ԭ����Ӧ��Zn+Ag2O+H2O�TZn��OH��2+2Ag���乤��ʾ��ͼ��ͼ������˵������ȷ���ǣ�������
��п�����һ�ֳ�����ѧ��Դ����ԭ����Ӧ��Zn+Ag2O+H2O�TZn��OH��2+2Ag���乤��ʾ��ͼ��ͼ������˵������ȷ���ǣ�������| A�� | Zn�缫�Ǹ��� | |
| B�� | Ag2O�缫�Ϸ�����ԭ��Ӧ | |
| C�� | Zn�缫�ĵ缫��Ӧʽ��Zn-2e-+2OH-�TZn��OH��2 | |
| D�� | �ŵ�ǰ��������Һ��pH���ֲ��� |
| A�� | ��0.1molCl2ȫ������ˮ�γɵ�1L��Һ�У�2c��Cl2��+c��Cl-��+c��HClO��+c��ClO-��=0.2mol•L-1 | |
| B�� | Na2CO3��Һ�У�c��OH-��-c��H+��=c��HCO3-��+c��H2CO3�� | |
| C�� | ���ʵ���Ũ�Ⱦ�Ϊ0.1mol•L-1��NaClO��NaHCO3�Ļ����Һ�У�c��HClO��+c��ClO-��=c��HCO3-��+c��H2CO3��+c��CO32-�� | |
| D�� | �����£���0.01mol•L-1��NH4HSO4��Һ�еμ�NaOH��Һ�����ԣ�c��Na+����c��SO42-����c��NH4+����c��OH-��=c��H+�� |
��1������ʼʱ����1mol N2��3mol H2���ﵽƽ�������a mol NH3
��2������ʼʱ��NH3��ֻ����N2��H2���ﵽƽ��ʱ����NH3�����ʵ���Ϊ3a mol����ʼʱ����N2��H2�����ʵ����ֱ�Ϊ��������
| A�� | 1mol��9mol | B�� | 2mol��9mol | C�� | 3mol��9mol | D�� | 3mol��6mol |
| A�� | �ڷ�Ӧ KClO3+6HCl�TKCl+3Cl2��+3H2O �У�Cl2���������������ǻ�ԭ������õ���״���µ� 67.2 L Cl2 ʱ����Ӧ��ת�Ƶĵ�����Ϊ 5NA | |
| B�� | ��״���£�22.4 L �ױ��к��е� C-H ����ĿΪ 8NA | |
| C�� | 50 g 46%���Ҵ�ˮ��Һ�У�����ԭ������ĿΪ 3NA | |
| D�� | t��ʱ��MgCO3�� Ksp=4��10-6������¶��±��� MgCO3��Һ�к��е� Mg2+��ĿΪ 2��10-3 NA |
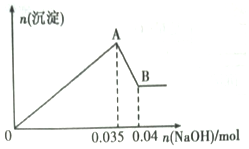 ij��ɫ��ҵ��ˮ�п��ܺ���Na+��Mg2+��Al3+��Cu2+��Cl-��SO42-�еļ������ӣ�
ij��ɫ��ҵ��ˮ�п��ܺ���Na+��Mg2+��Al3+��Cu2+��Cl-��SO42-�еļ������ӣ�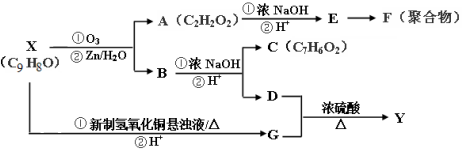
 ��
�� ��
�� ��
�� ��
��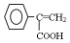 �����
��д���� Ϊ�л�ԭ�ϣ���ȡH�ĺϳ�·�ߣ�����ѡ��ԭ�ϣ���
Ϊ�л�ԭ�ϣ���ȡH�ĺϳ�·�ߣ�����ѡ��ԭ�ϣ���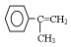 ��
��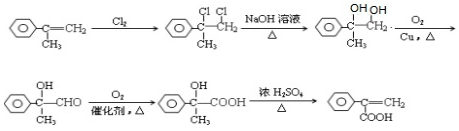 ��
��