题目内容
在强酸性溶液中能大量共存并且溶液为无色透明的离子组是( )
| A、Ca2+、Na+、NO3-、CO32- |
| B、Mg2+、Cl-、NH4+、SO42- |
| C、K+、Cl-、HCO3-、NO3- |
| D、Ca2+、Na+、Fe3+、NO3- |
考点:离子共存问题
专题:
分析:溶液无色,则有颜色的离子不能大量共存,溶液呈强酸性,存在大量的H+,如离子之间不发生任何反应,且与H+不反应,则可大量共存,以此解答该题.
解答:
解:A.在酸性条件下CO32-不能大量共存,故A错误;
B.溶液无色,且离子之间不发生任何反应,可大量共存,故B正确;
C.在酸性条件下HCO3-不能大量共存,故C错误;
D.Fe3+有颜色,不符合题目无色的要求,故D错误.
故选B.
B.溶液无色,且离子之间不发生任何反应,可大量共存,故B正确;
C.在酸性条件下HCO3-不能大量共存,故C错误;
D.Fe3+有颜色,不符合题目无色的要求,故D错误.
故选B.
点评:本题考查离子共存,为高频考点,侧重于学生的分析能力的考查,注意把握离子的性质以及反应类型的判断,本题注意酸性、无色的要求,难度不大.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
一定条件下,对于可逆反应X(g)+3Y(g)?2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1mol/L、0.3mol/L、0.08mol/L,则下列判断不正确的是( )
| A、c1:c2=1:3 |
| B、该反应一定是朝正向反应建立平衡 |
| C、X、Y的转化率相等 |
| D、c1的取值范围为0<c1<0.14 mol/L |
 某环保兴趣小组在处理污水样品时,需用质量分数为37%的浓盐酸(密度为1.19g/cm3)配制成250mL0.1mol?L-1的盐酸溶液.
某环保兴趣小组在处理污水样品时,需用质量分数为37%的浓盐酸(密度为1.19g/cm3)配制成250mL0.1mol?L-1的盐酸溶液.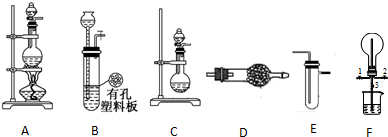
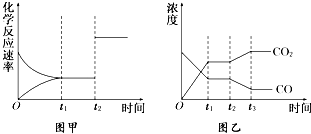 已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;
已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;