题目内容
(1)现有以下物质:①NaCl晶体 ②液态SO3 ③液态的醋酸 ④汞 ⑤BaSO4固体 ⑥纯蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧浓硫酸,
请回答下列问题(用序号):属于电解质的是 ,溶于水后形成的水溶液能导电的是 .
(2)胶体是一种常见的分散系,回答下列问题.
①向煮沸的蒸馏水中逐滴加入 溶液,继续煮沸至 ,停止加热,可制得Fe(OH)3胶体.
②区分胶体和溶液常用的方法叫做 .
请回答下列问题(用序号):属于电解质的是
(2)胶体是一种常见的分散系,回答下列问题.
①向煮沸的蒸馏水中逐滴加入
②区分胶体和溶液常用的方法叫做
考点:电解质与非电解质,胶体的重要性质
专题:
分析:(1)电解质:在水溶液中或熔融状态下能够导电的化合物;非电解质:在熔融状态和水溶液中都不能导电的化合物;
(2)①根据Fe(OH)3胶体的制备过程进行判断;
②根据胶体、溶液的性质判断,胶体具有丁达尔效应,而溶液不具备该性质.
(2)①根据Fe(OH)3胶体的制备过程进行判断;
②根据胶体、溶液的性质判断,胶体具有丁达尔效应,而溶液不具备该性质.
解答:
解:(1)①NaCl晶体在水溶液中能够导电,是电解质,
②液态SO3在水溶液中能够导电,但自身不能电离,是非电解质,
③液态的醋酸在水溶液中能够导电,是电解质,
④汞为金属单质,不溶于水,既不是电解质也不是非电解质,
⑤BaSO4固体不溶于水,在熔融状态下能够导电,是电解质,
⑥纯蔗糖(C12H22O11)在熔融状态和水溶液中都不能导电,是非电解质,
⑦酒精(C2H5OH)在熔融状态和水溶液中都不能导电,是非电解质,
⑧浓硫酸在水溶液中能够导电,但是混合物,既不是电解质也不是非电解质;
故属于电解质的是:①③⑤,溶于水后形成的水溶液能导电的是:①②③⑧;
故答案为:①③⑤;①②③⑧;
(2)①Fe(OH)3胶体的制备过程:向煮沸的蒸馏水中逐滴加入FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,
故答案为:FeCl3饱和;溶液呈红褐色;
②溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现光亮光路,为丁达尔现象,可以区别溶液和胶体,
故答案为:丁达尔效应.
②液态SO3在水溶液中能够导电,但自身不能电离,是非电解质,
③液态的醋酸在水溶液中能够导电,是电解质,
④汞为金属单质,不溶于水,既不是电解质也不是非电解质,
⑤BaSO4固体不溶于水,在熔融状态下能够导电,是电解质,
⑥纯蔗糖(C12H22O11)在熔融状态和水溶液中都不能导电,是非电解质,
⑦酒精(C2H5OH)在熔融状态和水溶液中都不能导电,是非电解质,
⑧浓硫酸在水溶液中能够导电,但是混合物,既不是电解质也不是非电解质;
故属于电解质的是:①③⑤,溶于水后形成的水溶液能导电的是:①②③⑧;
故答案为:①③⑤;①②③⑧;
(2)①Fe(OH)3胶体的制备过程:向煮沸的蒸馏水中逐滴加入FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,
故答案为:FeCl3饱和;溶液呈红褐色;
②溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现光亮光路,为丁达尔现象,可以区别溶液和胶体,
故答案为:丁达尔效应.
点评:本题考查电解质和非电解质的概念、物质的导电性、胶体的制备及性质,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
相关题目
下列物质的分类合理的是( )
| A、碱性氧化物:Na2O、CaO、MgO、CO2 |
| B、碱:纯碱、烧碱、熟石灰、苛性钠 |
| C、铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3?H2O |
| D、氧化物:CO2、NO、SO2、H2O |
用电石浆(主要成分是CaO、SiO2、Al2O3、Fe2O3、MgO、CaS 和其它不溶于酸的物质)生产无水CaCl2,工艺流程如下(已知氯化钙晶体的化学式是:CaCl2?6H2O),下列有关说法不正确的是( )
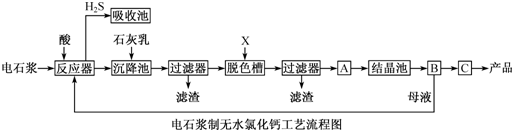

| A、反应器中加入的酸只能是盐酸 |
| B、脱色槽中应加入的X是为了脱色,所以可以选择活性炭或者过氧化钠 |
| C、氯化钙晶体CaCl2?6H2O可以直接脱水干燥得到无水CaCl2,无需在氯化氢的氛围下进行 |
| D、对设备B中产生的母液重新引入反应器,可以降低废弃物排放量,提高经济效益 |
在强酸性溶液中能大量共存并且溶液为无色透明的离子组是( )
| A、Ca2+、Na+、NO3-、CO32- |
| B、Mg2+、Cl-、NH4+、SO42- |
| C、K+、Cl-、HCO3-、NO3- |
| D、Ca2+、Na+、Fe3+、NO3- |