题目内容
19.(1)除去下列物质中所含少量杂质,填写所选用的试剂和分离方法| 混合物 (括号内为少量杂质) | 试剂 (足量) | 分离方法 | |
| A | 苯(苯酚) | ||
| B | 乙酸乙酯(乙酸) | ||
| C | 乙醇(水) |
①不能与金属钠反应
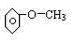 .
.②能与钠反应,但遇FeCl3不显色
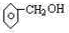 .
.③能与钠反应且遇FeCl3显紫色
 .
.
分析 (1)A.苯酚与NaOH反应后,与苯分层;
B.乙酸与饱和碳酸钠反应后,与乙酸乙酯分层;
C.CaO与水反应后,增大与乙醇的沸点差异;
(2)该分子的不饱和键=$\frac{7×2+2-8}{2}$=4,苯环相当于4个不饱和键,
①不能与金属钠反应,说明该物质不含羟基,则该物质为醚;
②能与钠反应,但遇FeCl3不显色则该物质为醇;
③能与钠反应且遇FeCl3显紫色,则该物质含有甲基和酚羟基.
解答 解:A.苯酚与NaOH反应后,与苯分层,则试剂为NaOH溶液,分离方法为分液;
B.乙酸与饱和碳酸钠反应后,与乙酸乙酯分层,则试剂为饱和碳酸钠溶液,分离方法为分液;
C.CaO与水反应后,增大与乙醇的沸点差异,则试剂为CaO,分离方法为蒸馏,
故答案为:
| 混合物 (括号内为少量杂质) | 试剂 (足量) | 分离方法 | |
| A | 苯(苯酚) | NaOH溶液 | 分液 |
| B | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 分液 |
| C | 乙醇(水) | CaO(生石灰)固体 | 蒸馏 |
(2)该分子的不饱和键=$\frac{7×2+2-8}{2}$=4,苯环相当于4个不饱和键,
①不能与金属钠反应,说明该物质不含羟基,则该物质为醚,则该有机物结构简式为
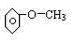 ,故答案为:
,故答案为: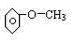 ;
;②能与钠反应,但遇FeCl3不显色则该物质为醇,其结构简式为
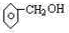 ,故答案为:
,故答案为: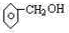 ;
;③能与钠反应且遇FeCl3显紫色,则该物质含有甲基和酚羟基,其结构简式为
 ,故答案为:
,故答案为: .
.点评 本题考查有机物的结构与性质及混合物分离提纯,为高频考点,把握有机物的组成、性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的综合应用,题目难度不大.

练习册系列答案
相关题目
9.合金具有许多优良的物理、化学或机械性能.下列物质不属于合金的是( )
| A. | 青铜 | B. | 钢 | C. | 硬铝 | D. | 玻璃 |
10.设NA为阿伏加德罗常数,下列有关说法正确的是( )
| A. | 1 mol甲基(-CH3)所含的电子总数为9NA | |
| B. | 1mol甲烷最多与2molCl2发生取代反应 | |
| C. | 标准状况下,2.24L乙醇含有的分子数目为0.1NA | |
| D. | 0.5 mol苯分子中含有C=C双键数为1.5 NA |
14.室温下,在pH=12的某溶液中,由水电离的c(OH-)为( )
①1.0×10-7 mol•L-1 ②1.0×10-6 mol•L-1 ③1.0×10-2 mol•L-1 ④1.0×10-12 mol•L-1.
①1.0×10-7 mol•L-1 ②1.0×10-6 mol•L-1 ③1.0×10-2 mol•L-1 ④1.0×10-12 mol•L-1.
| A. | ③ | B. | ④ | C. | ①③ | D. | ③④ |
8.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,2.24L苯含有的分子数为0.1NA | |
| B. | 常温常压下,18g H2O含有10nA个电子 | |
| C. | 1L1mol•L-1的NH4Cl溶液中有nA个NH4+ | |
| D. | 一定条件下,向密闭容器中投入3mol H2和1mol N2充分反应后可得到NH3分子数为2NA |