题目内容
某工业废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO42-.若取这种废液来制取较纯净的氯化钾晶体及液溴(Br2)可设计如下流程:
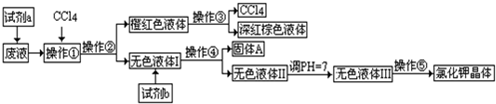
可供试剂a、b的选择试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2、KMnO4(H+)溶液、稀HNO3.
(1)试剂a应该选用 ;
(2)操作①、②、③、④、⑤的名称是 (选填字母编号).
a.萃取、过滤、分液、过滤、蒸发结晶
b.萃取、分液、蒸馏、过滤、蒸发结晶
c.分液、萃取、过滤、过滤、蒸发结晶
d.萃取、分液、分液、过滤、蒸发结晶
(3)除去无色液体I中的Ca2+、Mg2+、SO42-离子,选出b所代表的试剂,按滴加顺序依次是 (填写化学式).
(4)调节pH的作用是 ,操作方法是 .
(5)操作⑤中用到的瓷质仪器名称是 .
(6)如果用电解氯化钾溶液来制取氢气和氯气,再使氢气与氯气反应生成氯化氢,将生成的氯化氢用水吸收制得盐酸.为了制得100吨35%的盐酸,理论上需氯化钾 吨.

可供试剂a、b的选择试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2、KMnO4(H+)溶液、稀HNO3.
(1)试剂a应该选用
(2)操作①、②、③、④、⑤的名称是
a.萃取、过滤、分液、过滤、蒸发结晶
b.萃取、分液、蒸馏、过滤、蒸发结晶
c.分液、萃取、过滤、过滤、蒸发结晶
d.萃取、分液、分液、过滤、蒸发结晶
(3)除去无色液体I中的Ca2+、Mg2+、SO42-离子,选出b所代表的试剂,按滴加顺序依次是
(4)调节pH的作用是
(5)操作⑤中用到的瓷质仪器名称是
(6)如果用电解氯化钾溶液来制取氢气和氯气,再使氢气与氯气反应生成氯化氢,将生成的氯化氢用水吸收制得盐酸.为了制得100吨35%的盐酸,理论上需氯化钾
考点:物质的分离、提纯和除杂
专题:实验题,离子反应专题
分析:(1)试剂a能将Br-氧化为Br2,试剂a应具有氧化性;
(2)无色液体Ⅰ中含有K+、Cl-、Ca2+、Mg2+、SO42-,无色液体Ⅲ中只含有K+、Cl-,则试剂b的作用是除去Ca2+、Mg2+、SO42-;
(3)除去Ca2+,选用饱和K2CO3溶液;除去Mg2+,选用KOH溶液;除去SO42-,选用BaCl2溶液;
(4)无色液体Ⅱ中还含有杂质离子CO32-和OH-;用pH试纸测定至pH=7;
(5)操作⑤是蒸发结晶;
(6)根据氯元素守恒解题.
(2)无色液体Ⅰ中含有K+、Cl-、Ca2+、Mg2+、SO42-,无色液体Ⅲ中只含有K+、Cl-,则试剂b的作用是除去Ca2+、Mg2+、SO42-;
(3)除去Ca2+,选用饱和K2CO3溶液;除去Mg2+,选用KOH溶液;除去SO42-,选用BaCl2溶液;
(4)无色液体Ⅱ中还含有杂质离子CO32-和OH-;用pH试纸测定至pH=7;
(5)操作⑤是蒸发结晶;
(6)根据氯元素守恒解题.
解答:
解:(1)由加入的CCl4及得到的深红棕色液体知,试剂a能将Br-氧化为Br2,试剂a应具有氧化性,所以应选用H2O2溶液,故答案为:H2O2溶液;
(2)由流程图知,无色液体Ⅰ中含有K+、Cl-、Ca2+、Mg2+、SO42-,无色液体Ⅲ中只含有K+、Cl-,则试剂b的作用是除去Ca2+、Mg2+、SO42-.操作①是萃取,操作②是将互不相溶的两种液体分开-分液,操作③是将沸点不同的、互溶的两液体分开-蒸馏,操作④是将溶液与沉淀分开-过滤,操作⑤是将KCl从其水溶液中提取出来-结晶,故答案为:b;
(3)由于除杂时除杂试剂需过量,且不能引入新杂质,所以除去Ca2+,选用饱和K2CO3溶液;除去Mg2+,选用KOH溶液;除去SO42-,选用BaCl2溶液.而且只要满足BaCl2溶液在饱和K2CO3溶液之前加入即可,
故答案为:BaCl2溶液、饱和K2CO3溶液、KOH溶液(或KOH溶液、BaCl2溶液、饱和K2CO3溶液或BaCl2溶液、KOH溶液、饱和K2CO3溶液);
(4)由以上知,无色液体Ⅱ中还含有杂质离子CO32-和OH-,需用盐酸来除去过量的OH-及CO32-,调节pH=7的操作方法是滴加盐酸,无气体产生时,用pH试纸测定至pH=7,
故答案为:除去过量的OH-及CO32-;滴加稀盐酸,无气体产生时,用pH试纸测定至pH=7;
(5)由于操作⑤是蒸发结晶,所以该操作用到的瓷质仪器是蒸发皿,故答案为:蒸发皿;
(6)氯化氢的物质的量与氯化钾的物质的量相等,100×35%×
=71.43吨,故答案为:71.43.
(2)由流程图知,无色液体Ⅰ中含有K+、Cl-、Ca2+、Mg2+、SO42-,无色液体Ⅲ中只含有K+、Cl-,则试剂b的作用是除去Ca2+、Mg2+、SO42-.操作①是萃取,操作②是将互不相溶的两种液体分开-分液,操作③是将沸点不同的、互溶的两液体分开-蒸馏,操作④是将溶液与沉淀分开-过滤,操作⑤是将KCl从其水溶液中提取出来-结晶,故答案为:b;
(3)由于除杂时除杂试剂需过量,且不能引入新杂质,所以除去Ca2+,选用饱和K2CO3溶液;除去Mg2+,选用KOH溶液;除去SO42-,选用BaCl2溶液.而且只要满足BaCl2溶液在饱和K2CO3溶液之前加入即可,
故答案为:BaCl2溶液、饱和K2CO3溶液、KOH溶液(或KOH溶液、BaCl2溶液、饱和K2CO3溶液或BaCl2溶液、KOH溶液、饱和K2CO3溶液);
(4)由以上知,无色液体Ⅱ中还含有杂质离子CO32-和OH-,需用盐酸来除去过量的OH-及CO32-,调节pH=7的操作方法是滴加盐酸,无气体产生时,用pH试纸测定至pH=7,
故答案为:除去过量的OH-及CO32-;滴加稀盐酸,无气体产生时,用pH试纸测定至pH=7;
(5)由于操作⑤是蒸发结晶,所以该操作用到的瓷质仪器是蒸发皿,故答案为:蒸发皿;
(6)氯化氢的物质的量与氯化钾的物质的量相等,100×35%×
| 74.5 |
| 36.5 |
点评:本题考查物质的分离、提纯,侧重于学生的分析能力、实验能力和评价能力的考查,难度不大,注意把握物质的性质的异同,注意除杂时不能引入新的杂质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2012-09-25安徽省机动车氮氧化物总量减排现场会召开,会议指出,要积极推进机动车污染防治.为了减轻大气污染,科学家正在研究利用催化技术将汽车尾气中的NO和CO转变成CO2和N2,即2NO+2CO?2CO2+N2△H<0若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
| A、单位时间内消耗CO和CO2.的物质的量相等时,反应达到平衡状态 |
| B、平衡时,其他条件不变,升高温度可提高CO的转化率 |
| C、使用高效催化剂,提高正反应速率、降低逆反应速率 |
| D、平衡前,随着反应的进行,容器内压强始终不变 |
 随着人们法律意识的增强,社会各界人士对食品安全问题关注也与日俱增,目前石家庄的“三鹿奶粉”事件是不法奶商向原奶中加入了三聚氰胺,其结构简式如图.下列关于三聚氰胺的说法正确的是( )
随着人们法律意识的增强,社会各界人士对食品安全问题关注也与日俱增,目前石家庄的“三鹿奶粉”事件是不法奶商向原奶中加入了三聚氰胺,其结构简式如图.下列关于三聚氰胺的说法正确的是( )| A、三聚氰胺分子中所有原子都在同一平面上 |
| B、三聚氰胺分子中含有不饱和碳原子,在一定条件下能发生加成反应 |
| C、三聚氰胺分子含氮量很高,含氮量高达38.1% |
| D、三聚氰胺分子具有一定的酸性,在一定的条件下能发生氧化反应 |
将金属钠分别投入下列物质的稀溶液中,一定能生成白色沉淀的是( )
| A、NaCl |
| B、Al2(SO4)3 |
| C、MgCl2 |
| D、CuSO4 |
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质,以下叙述正确的是( )
| A、植物通过光合作用将CO2转化成葡萄糖是太阳能转变成热能的过程 |
| B、油脂属于酯类化合物,油脂的水解反应叫皂化反应 |
| C、淀粉与纤维素互称为同分异构体 |
| D、浓硝酸溅在皮肤上,使皮肤呈黄色是由于浓硝酸和蛋白质发生了颜色反应 |
下列物质中,在一定条件下,既能发生银镜反应,又能发生水解反应的是( )
| A、葡萄糖 | B、麦芽糖 |
| C、溴乙酸 | D、甲酸钠 |
高温下,反应H2(g)+I2(g)?2HI(g)+Q,达到平衡时,要使混合气体的颜色加深,可采取的方法是( )
| A、缩小体积 | B、降低温度 |
| C、加入氩气 | D、增大氢气浓度 |

