题目内容
如图装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色.下列说法中不正确的是( )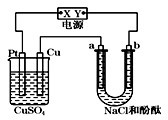

| A、X是正极,Y是负极 |
| B、X是负极,Y是正极 |
| C、CuSO4溶液的pH逐渐减小 |
| D、NaCl溶液的pH逐渐变大 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:通电电解氯化钠溶液时,b极附近溶液呈红色,说明b极生成氢氧根离子,则电解的是氢离子,所以b连接的Y为电源的负极,则X为正极,电解硫酸铜时,阳极上会产生氧气,阴极上会产生金属铜,根据电解方程式确定溶液pH的变化.
解答:
解:A、B、b极附近溶液呈红色,说明b极生成氢氧根离子,则电解的是氢离子,所以b连接的Y为电源的负极,则X为正极,故A正确,B错误;
C、通电电解硫酸铜时,总反应为:2CuSO4+2H2O
2Cu+2H2SO4+O2↑,电解生成硫酸,溶液的pH减小,故C正确;
D、通电电解NaCl溶液时,总反应为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,电解生成氢氧化钠,所以溶液的pH增大,故D正确.
故选B.
C、通电电解硫酸铜时,总反应为:2CuSO4+2H2O
| ||
D、通电电解NaCl溶液时,总反应为:2NaCl+2H2O
| ||
故选B.
点评:本题考查电解池的工作原理知识,题目难度不大,注意根据电极现象判断电源的正负极为解答该题的关键.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
等物质的量的下列物质,分别完全燃烧时,消耗氧气最少的是( )
| A、苯 | B、甲烷 | C、乙烯 | D、乙醇 |
下列选项中所涉及的两个量一定相等的是( )
| A、11.2 L N2与14 g CO气体所含有的原子数 |
| B、电解精炼铜时阳极溶解与阴极析出的铜的质量 |
| C、6.2 g Na2O和7.8 g Na2O2中所含的离子数 |
| D、1.8g重水(D2O,D为12H)中含有的中子数为6.02×1022 |
下列四类基本反应:①置换反应,②复分解反应,③化合反应,④分解反应.其中一定不是氧化还原反应的是( )
| A、只有② | B、②③ |
| C、②④ | D、②③④ |
完全沉淀等物质的量浓度的NaCl、MgCl2、AlCl3溶液中的Cl-,消耗等物质的量浓度的AgNO3溶液的体积比为2:3:6,则上述溶液的体积比为( )
| A、1:1:1 |
| B、3:2:1 |
| C、6:3:2 |
| D、4:3:4 |
以下四组物质的水溶液,其中仅用溶液间的两两混合,就可以完成鉴别任务的是( )
| A、MgCl2 Na2SO4 BaCl2 KOH |
| B、BaCl2 AgNO3 CaCl2 HNO3 |
| C、NaOH Na2SO4 KNO3 HCl |
| D、HCl Na2CO3 Na2SO4 BaCl2 |
反应A+B→C+D,若10g A和6g B恰好反应生成5g C,则5g A和4g B完全反应可生成D的质量为( )
| A、11g | B、5.5g |
| C、2.5g | D、无法确定 |
心脏起搏器电源-锂碘电池的电池反应为:2Li(s)+I2(s)=2LiI(s)△H
已知:4Li(s)+O2 (g)=2Li2O(s)△H1
4LiI(s)+O2(g)=2I2(s)+2Li2O(s)△H2
则下列说法正确的是( )
已知:4Li(s)+O2 (g)=2Li2O(s)△H1
4LiI(s)+O2(g)=2I2(s)+2Li2O(s)△H2
则下列说法正确的是( )
A、△H=
| ||||
B、△H=
| ||||
C、△H=
| ||||
D、△H=
|