题目内容
心脏起搏器电源-锂碘电池的电池反应为:2Li(s)+I2(s)=2LiI(s)△H
已知:4Li(s)+O2 (g)=2Li2O(s)△H1
4LiI(s)+O2(g)=2I2(s)+2Li2O(s)△H2
则下列说法正确的是( )
已知:4Li(s)+O2 (g)=2Li2O(s)△H1
4LiI(s)+O2(g)=2I2(s)+2Li2O(s)△H2
则下列说法正确的是( )
A、△H=
| ||||
B、△H=
| ||||
C、△H=
| ||||
D、△H=
|
考点:反应热和焓变
专题:化学反应中的能量变化
分析:利用盖斯定律解答即可,用盖斯定律解答,从待求反应出发,分析待求反应中的反应物和生成物在已知反应中的位置,通过相互加减可得.
解答:
解:已知:①4Li(s)+O2 (g)=2Li2O(s)△H1
②4LiI(s)+O2(g)=2I2(s)+2Li2O(s)△H2
据盖斯定律(①-②)÷2得:2Li(s)+I2(s)=2LiI(s)△H=
H1-
△H2,
故选:C.
②4LiI(s)+O2(g)=2I2(s)+2Li2O(s)△H2
据盖斯定律(①-②)÷2得:2Li(s)+I2(s)=2LiI(s)△H=
| 1 |
| 2 |
| 1 |
| 2 |
故选:C.
点评:有关盖斯定律的习题,首先要根据所求的反应分析,分析以下几点:
1、所求反应中的反应物在哪个反应了?是反应物还是生成物?
2、所给反应中哪些物质是所求反应中没有的?
3、如何才能去掉无用的?然后,通过相互加减,去掉无关物质.
将所对应的△H代入上述化学方程式的加减中就可以了.
1、所求反应中的反应物在哪个反应了?是反应物还是生成物?
2、所给反应中哪些物质是所求反应中没有的?
3、如何才能去掉无用的?然后,通过相互加减,去掉无关物质.
将所对应的△H代入上述化学方程式的加减中就可以了.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
如图装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色.下列说法中不正确的是( )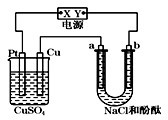

| A、X是正极,Y是负极 |
| B、X是负极,Y是正极 |
| C、CuSO4溶液的pH逐渐减小 |
| D、NaCl溶液的pH逐渐变大 |
已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3kJ/mol,则下列说法中正确的是( )
| A、浓硫酸和NaOH溶液反应,生成1mol水时放热57.3kJ |
| B、含1mol H2SO4的稀硫酸与足量稀NaOH溶液中和后,放热为57.3 kJ |
| C、1L 0.1mol/L CH3COOH与1L 0.1mol/L NaOH溶液反应后放热为5.73 kJ |
| D、1L 0.1 mol/L HNO3与1L 0.1mol/L NaOH溶液反应后放热为5.73 kJ |
在由水电离出的c(H+)=10-13mol?L-1的溶液中一定能够大量存在的离子组是( )
| A、Ba2+、Na+、Cl-、NO3- |
| B、Al3+、Ca2+、SO42-、Br- |
| C、NH4+、K+、HSO3-、CO32- |
| D、Na+、K+、Cl-、I- |
分别在等体积等pH或等物质的量浓度的盐酸和醋酸溶液中,加入足量锌粉,氢离子浓度c(H+)及氢气的体积V(H2)(同温同压下测定)的变化图示如下,其中正确的是( ) 

| A、①②③ | B、②④ |
| C、①③ | D、①②③④ |
下列能表示阿伏加德罗常数数值的是( )
| A、1molH2含有的电子数 |
| B、通常状况下,22.4LCO2所含的分子数 |
| C、0.012kg12C所含的原子数 |
| D、1LO.5mol?L-1的CaCl2溶液所含的Cl-数 |
下列反应既属于氧化还原反应,又属于化合反应的是( )
A、2Fe+3Cl2
| ||||
B、Fe2O3+3CO
| ||||
| C、CaO+CO2═CaCO3 | ||||
| D、H2SO4+2NaOH═Na2SO4+2H2O |
下列实验能达到预期目的是( )
| A、用乙醇萃取碘水中的碘 |
| B、用通入适量O2并点燃的方法除去CO2中混有的少量CO杂质 |
| C、向煮沸的1 mol?L-1 NaOH溶液中滴加FeCl3饱和溶液制备Fe(OH)3胶体 |
| D、向混有碳酸钾的氯化钾溶液中加入适量的盐酸,除去其中的碳酸钾 |