题目内容
下列选项中所涉及的两个量一定相等的是( )
| A、11.2 L N2与14 g CO气体所含有的原子数 |
| B、电解精炼铜时阳极溶解与阴极析出的铜的质量 |
| C、6.2 g Na2O和7.8 g Na2O2中所含的离子数 |
| D、1.8g重水(D2O,D为12H)中含有的中子数为6.02×1022 |
考点:物质的量的相关计算,电解原理
专题:计算题
分析:A.温度和压强未知,无法计算氮气的物质的量;
B.电解精炼粗铜时,阳极溶解的铜小于阴极析出的铜;
C.氧化钠和过氧化钠化学式中阴阳离子个数相等;
D.一个重水分子中含有10个中子,1.8g重水的物质的量=
=0.9mol,水分子数为0.9NA.
B.电解精炼粗铜时,阳极溶解的铜小于阴极析出的铜;
C.氧化钠和过氧化钠化学式中阴阳离子个数相等;
D.一个重水分子中含有10个中子,1.8g重水的物质的量=
| 1.8g |
| 20g/mol |
解答:
解:A.温度和压强未知,无法计算氮气的物质的量,14gCO的物质的量=
=0.5mol,所以其含有的原子个数不一定相等,故A错误;
B.电解精炼粗铜时,阳极上铜和其它金属溶解,阴极上析出铜,根据转移电子相等知,阳极溶解的铜小于阴极析出的铜,故B错误;
C.氧化钠和过氧化钠化学式中阴阳离子个数相等,6.2 g Na2O的物质的量=
=0.1mol,7.8 g Na2O2的物质的量=
=0.1mol,所以6.2 g Na2O和7.8 g Na2O2中所含的离子数相等,故C正确;
D.一个重水分子中含有10个中子,1.8g重水的物质的量=
=0.9mol,水分子数为0.9NA,则1.8g重水(D2O,D为12H)中含有的中子数为9×6.02×1023,故D错误;
故选C.
| 14g |
| 28g/mol |
B.电解精炼粗铜时,阳极上铜和其它金属溶解,阴极上析出铜,根据转移电子相等知,阳极溶解的铜小于阴极析出的铜,故B错误;
C.氧化钠和过氧化钠化学式中阴阳离子个数相等,6.2 g Na2O的物质的量=
| 6.2g |
| 62g/mol |
| 7.8g |
| 78g/mol |
D.一个重水分子中含有10个中子,1.8g重水的物质的量=
| 1.8g |
| 20g/mol |
故选C.
点评:本题考查了物质的量的计算、电解原理等知识点,根据物质构成、电解原理、基本公式等知识点来分析解答,注意气体摩尔体积的适用范围及适用条件,知道过氧化钠、氧化钠的构成微粒,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于氧化物的叙述正确的是( )
| A、能和强酸溶液反应的氧化物就是碱性氧化物 |
| B、不能跟碱反应的氧化物一定能和酸反应 |
| C、金属氧化物一定是碱性氧化物 |
| D、酸性氧化物不一定都能与水反应生成酸 |
反应4A(s)+3B(g)═2C(g)+D(g),经2min,B的浓度减少0.6mol?L-1,对此反应速率的表示,正确的是( )
| A、A的浓度减少了0.8mol?L-1 |
| B、分别用B、C、D表示的反应速率其比值为1:1:1 |
| C、在2min末的反应速率,用B表示是0.3mol?L-1?min-1 |
| D、在这2min内用B和C表示的反应速率都是逐渐减小的 |
随着社会的发展,人们日益重视环境问题、节能减排,下列说法不正确的是( )
| A、绿色化学的核心是利用化学原理从源头上减少和消除工农业生产等对环境的污染 |
| B、“低碳生活”倡导生活中耗用能量尽量减少,从而减少CO2排放 |
| C、采用催化转换技术将汽车尾气中的NOx和CO转化为无毒气体 |
| D、大量进口国外电子垃圾,回收其中的贵重金属 |
下列物质既有氧化性又有还原性的是( )
| A、HCl |
| B、Fe |
| C、Cl- |
| D、Na+ |
如图装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色.下列说法中不正确的是( )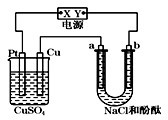

| A、X是正极,Y是负极 |
| B、X是负极,Y是正极 |
| C、CuSO4溶液的pH逐渐减小 |
| D、NaCl溶液的pH逐渐变大 |
为了配制c(NH4+):c(C1-)=1:1的NH4C1溶液,可在NH4C1溶液中加入( )
①适量的HCl ②适量的NaCl ③适量的氨水
④适量的NaOH ⑤加水 ⑥适量的(NH4)2CO3.
①适量的HCl ②适量的NaCl ③适量的氨水
④适量的NaOH ⑤加水 ⑥适量的(NH4)2CO3.
| A、③ | B、①②③④ |
| C、⑤⑥ | D、②③⑥ |
在由水电离出的c(H+)=10-13mol?L-1的溶液中一定能够大量存在的离子组是( )
| A、Ba2+、Na+、Cl-、NO3- |
| B、Al3+、Ca2+、SO42-、Br- |
| C、NH4+、K+、HSO3-、CO32- |
| D、Na+、K+、Cl-、I- |