题目内容
NH4+的摩尔质量是 ;含71g Na2SO4的溶液中,Na+和SO42-的物质的量分别是 和 .
考点:摩尔质量,物质的量的相关计算
专题:阿伏加德罗常数和阿伏加德罗定律
分析:摩尔质量是单位物质的量的物质质量,数值上等于相对分子(原子)质量;依据n=
计算物质的量,结合化学式计算离子物质的量.
| m |
| M |
解答:
解:NH4+的摩尔质量是18g/mol,含71g Na2SO4的溶液中,n(Na2SO4)=
=0.5mol,Na+和SO42-的物质的量分别是1mol,0.5mol;
故答案为:18g/mol;1mol;0.5mol.
| 71g |
| 142g/mol |
故答案为:18g/mol;1mol;0.5mol.
点评:本题考查了摩尔质量概念分析,物质的量和质量的换算,掌握概念实质是关键,题目较简单.

练习册系列答案
相关题目
下列关于氧化物的叙述正确的是( )
| A、能和强酸溶液反应的氧化物就是碱性氧化物 |
| B、不能跟碱反应的氧化物一定能和酸反应 |
| C、金属氧化物一定是碱性氧化物 |
| D、酸性氧化物不一定都能与水反应生成酸 |
如图装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色.下列说法中不正确的是( )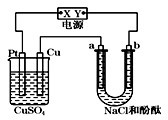

| A、X是正极,Y是负极 |
| B、X是负极,Y是正极 |
| C、CuSO4溶液的pH逐渐减小 |
| D、NaCl溶液的pH逐渐变大 |

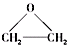 ),该反应的原子利用率为100%,反应的化学方程式为
),该反应的原子利用率为100%,反应的化学方程式为