��Ŀ����
2�� �״�����Ҫ�Ļ���ԭ�ϣ��ֿɳ�Ϊȼ�ϣ���ҵ�����úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ����������ºϳɼ״�����������Ҫ��Ӧ���£�
�״�����Ҫ�Ļ���ԭ�ϣ��ֿɳ�Ϊȼ�ϣ���ҵ�����úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ����������ºϳɼ״�����������Ҫ��Ӧ���£���CO��g��+2H2��g���TCH3OH��g����H
��CO2��g��+3H2��g���TCH3OH��g��+H2O��g����H2=-58kJ•mol-1
��CO2��g��+H2��g���TCO��g��+H2O��g����H3=+41kJ•mol-1
�ش��������⣺
��1����֪��Ӧ���е���صĻ�ѧ�������������£�
| ��ѧ�� | H�TH | C�TO | C��O | H-O | C-H |
| F/��kJ•mol-1�� | 435 | 343 | 1076 | 465 | X |
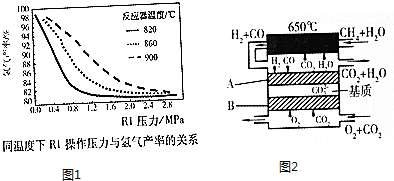
��2����T��ʱ��6molCO2��8molH2����2L�ܱ������з�����Ӧ�ڣ����H2�����ʵ�����ʱ��仯��ϵ��ͼ��״̬I��ͼ��ʵ�ߣ���ʾ��ͼ������A��1��6��������1minʱH2�����ʵ�����6mol��
��T��ʱ״̬I�����£�0��3min��CH3OH��ƽ����Ӧ����v=0.28mol/��L•min����ƽ�ⳣ��K=0.5��
��������������ʱ�����ı�ijһ��������H2�����ʵ�����ʱ��仯��ͼ��״̬����ʾ����ı����������������ѹǿ��
�������������䣬���ı��¶�ʱ�����H2�����ʵ�����ʱ��仯��ͼ��״̬����ʾ����״̬���Ӧ���¶ȣ������������������=����T�棻
����״̬���ƽ�ⳣ��ΪK2��״̬���ƽ�ⳣ��ΪK3����K2�������������������=����K3��
��һ���¶���ͬ���˷�Ӧ�ں��������н��У����жϸ÷�Ӧ�ﵽ��ѧƽ�����ݵ���ac��
a��������ѹǿ���� b���״���ˮ����������ȱ��ֲ���
c��v����H2��=3v����CH3OH�� d��2��C�TO���ѵ�ͬʱ��6��H-H���ѣ�
���� ��1����֪����CO��g��+2H2��g��?CH3OH��g����H
��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-58kJ/mol
��CO2��g��+H2��g��?CO��g��+H2O��g����H=+41kJ/mol
���ݸ�˹���ɣ���-��=�٣��ݴ˼����H���ٽ�ϼ��ܼ���x��
��2���ٸ��ݷ�Ӧ���ʵļ��㹫ʽ���м���0��3min��CH3OH��ƽ����Ӧ���ʣ�����ͼ���֪����Ӧ��8min�ﵽƽ�⣬��ʱ���������ʵ���Ϊ2mol��������ʽ�����㻯ѧƽ�ⳣ��K��
�ڢ���4min�ﵽƽ�⣬��ƽ��ʱ���������ʵ����Ȣ�С��˵����Ӧ���ʼӿ죬��ƽ�������ƶ����ٸ���Ӱ�컯ѧƽ������ط����ɵã�
��״̬��Ӧ���ʿ죬ƽ��ʱ���������ʵ����Ϣ��˵��ƽ�������ƶ������¶������ˣ�
�ܸ����¶ȶԻ�ѧƽ����ƶ��ɵ�K�Ĵ�С��
�ݿ��淴Ӧƽ��ʱ�����淴Ӧ������ȣ�����ֺ������ֲ��䣬�ݴ˷�����
��� �⣺��1����֪����CO��g��+2H2��g��?CH3OH��g����H
��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-58kJ/mol
��CO2��g��+H2��g��?CO��g��+H2O��g����H=+41kJ/mol
���ݸ�˹���ɣ���-��=�٣�����еġ�H=-58kJ/mol-41kJ/mol=-99kJ/mol��
��ʱ��H=��Ӧ��ļ��ܺ�-������ļ��ܺ�=��1076kJ•mol-1+435��2kJ•mol-1��-��xkJ•mol-1��3+465kJ•mol-1+343kJ•mol-1��=-99kJ/mol�����x=413��
�ʴ�Ϊ��413��
��2����T��ʱ״̬I�����£�3minʱH2�����ʵ���Ϊ3mol���仯5mol�����ݷ�Ӧ CO2��g��+3H2��g��?CH3OH��g��+H2O��g����֪CH3OH��g���ı仯���ʵ���Ϊ$\frac{5}{3}$mol����ʱ0��3min��CH3OH��ƽ����Ӧ����v=$\frac{��\frac{\frac{5}{3}mol}{2L}��}{3min}$��0.28mol/��L•min����
T��ʱ��6molCO2��8molH2����2L�ܱ������з�����Ӧ�ڣ�����ͼ���֪����Ӧ��8min�ﵽƽ�⣬��ʱ���������ʵ���Ϊ2mol��������ʽ��
CO2��g��+3H2��g��?CH3OH��g��+H2O��g��
��ʼ��mol/L����3 4 0 0
ת����mol/L����1 3 1 1
ƽ�⣨mol/L����2 1 1 1
��Ӧ�ڵ�ƽ�ⳣ��K=$\frac{1��1}{2��{1}^{3}}$=0.5��
�ʴ�Ϊ��0.28mol/��L•min����0.5��
�ڴ�ͼ���֪������4min�ﵽƽ�⣬˵����Ӧ���ʼӿ죬��Ϊ�����¶ȣ��Ӵ���������ѹǿ��ƽ��ʱ���������ʵ����Ȣ�С��˵��ƽ�������ƶ����÷�Ӧ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���������Ӱ��ƽ�⣬�÷�Ӧ�Ǹ����������С�ķ�Ӧ������ѹǿ��ƽ�������ƶ�����Ӧ��������ѹǿ��
�ʴ�Ϊ������ѹǿ��
�۸���ͼ��״̬��ﵽƽ��������ʱ��̣���Ӧ���ʽϿ죬ƽ��ʱ���������ʵ���Ҳ�ϴ�˵����Ӧ�����ƶ�����Ӧ�¶Ƚ�T��ߣ�
�ʴ�Ϊ������
��״̬������ѹǿ���¶Ȳ��䣬��ΪT�棬״̬���¶ȱ�T��ߣ��÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ���¶����ߣ�ƽ�������ƶ�����ѧƽ�ⳣ����С��K2��K3��
�ʴ�Ϊ������
�ݷ�ӦCO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-58kJ/mol�ں��������н��У�
a����Ӧ���������С������ʱ�����ŷ�Ӧ�Ľ��У�ѹǿ��С��ƽ���������ѹǿ���ֲ��䣬��a��ȷ��
b���״���ˮ������Ϊ����������ʼ��δ1��1���ֲ��䣬��b����
c��v����H2��=3v����CH3OH��=3v����CH3OH�������淴Ӧ������ȣ���Ӧƽ�⣬��c��ȷ��
d���κ�ʱ�̣�2��C=O���ѵ�ͬʱ����6��H-H���ѣ���d����
�ʴ�Ϊ��ac��
���� ���⿼���˸�˹���ɡ���ѧƽ�ⳣ���ļ��㣬Ӱ�컯ѧƽ��������Լ���ѧƽ��״̬���жϣ���Ŀ�ѶȲ������ڿ���Ի���֪ʶ���������գ�

| A�� | �������� | B�� | �������� | C�� | ������ | D�� | �Ȼ��� |
| t/s | 0 | 500s | 1 000s |
| c��H2��/��mol•L-1�� | 5.00 | 3.52 | 2.48 |
| c��CO��/��mol•L-1�� | 2.50 |
��2����1 000 s����CO��ʾ�Ļ�ѧ��Ӧ������0.00126mol•L-1•s-1��1 000sʱH2��ת������50.4%��
��3����500sʱ���ɵļ״���Ũ����0.74mol•L-1��
| A�� | ���ۺ͵���ø��Ϻ��� | |
| B�� | ��պ����������Ϊ75%�ľƾ������Ƥ�� | |
| C�� | �������߹�����䲡�� | |
| D�� | �ø������ֽ�����걾 |
| A�� | �������������ߵ�λʱ�䰱�IJ��� | |
| B�� | ��ѹ�����ڰ��ĺϳɷ�Ӧ | |
| C�� | 500����±����¸������ںϳɰ��ķ�Ӧ | |
| D�� | ���º����£��ںϳɰ�ƽ����ϵ�г���He��ʹѹǿ������ƽ�������ƶ���NH3���� |
C��s��+O2��g���TCO2��g����H=-Q2 kJ•mol-1��
S��s��+O2��g���TSO2��g����H=-Q3 kJ•mol-1��
CO������Ӧ������������ж���Ϊ��ֹ�������ж�����ҵ�ϳ���SO2��CO��������������ת��Ϊ��������÷�Ӧ���Ȼ�ѧ����ʽΪ��������
| A�� | SO2��g��+2CO��g���TS��s��+2CO2��g����H=��2Q1-2Q2+Q3�� kJ•mol-1 | |
| B�� | S��s��+2CO��g���TSO2��g��+2C��s����H=��Q1-Q3�� kJ•mol-1 | |
| C�� | SO2��g��+2CO��g���TS��s��+2CO2��g����H=��Q1-2Q2+Q3�� kJ•mol-1 | |
| D�� | SO2��g��+2CO��g���TS��s��+2CO2��g����H=��2Q1-Q2+2Q3�� kJ•mol-1 |
| A�� | ������������ | B�� | ������Һ��ǿ����Һ��Ӧ | ||
| C�� | ǿ����Һ��ǿ����Һ��Ӧ | D�� | ��Ԫǿ����Һ��һԪǿ����Һ��Ӧ |