题目内容
11.已知:2C(s)+O2(g)═2CO(g)△H=-Q1 kJ•mol-1;C(s)+O2(g)═CO2(g)△H=-Q2 kJ•mol-1;
S(s)+O2(g)═SO2(g)△H=-Q3 kJ•mol-1.
CO与镍反应会造成镍催化剂中毒,为防止镍催化剂中毒,工业上常用SO2将CO氧化,二氧化硫转化为单质硫,则该反应的热化学方程式为( )
| A. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(2Q1-2Q2+Q3) kJ•mol-1 | |
| B. | S(s)+2CO(g)═SO2(g)+2C(s)△H=(Q1-Q3) kJ•mol-1 | |
| C. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(Q1-2Q2+Q3) kJ•mol-1 | |
| D. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(2Q1-Q2+2Q3) kJ•mol-1 |
分析 用SO2将CO氧化,二氧化硫转化为单质硫,反应的化学方程式为SO2(g)+2CO(g)═S(s)+2CO2(g),已知①2C(s)+O2(g)═2CO(g)△H=-Q1 kJ•mol-1;②C(s)+O2(g)═CO2(g)△H=-Q2 kJ•mol-1;③S(s)+O2(g)═SO2(g)△H=-Q3 kJ•mol-1,将②×2-①-③可得SO2将CO氧化,二氧化硫转化为单质硫的热化学方程式.
解答 解:用SO2将CO氧化,二氧化硫转化为单质硫,反应的化学方程式为SO2(g)+2CO(g)═S(s)+2CO2(g),
已知①2C(s)+O2(g)═2CO(g)△H=-Q1 kJ•mol-1;
②C(s)+O2(g)═CO2(g)△H=-Q2 kJ•mol-1;
③S(s)+O2(g)═SO2(g)△H=-Q3 kJ•mol-1,
将②×2-①-③可得SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(Q1-2Q2+Q3) kJ•mol-1,
故选C.
点评 该题考查热化学方程式的书写、反应热的计算,是高考中的常见题型,试题基础性强,难易适中.有利于培养学生学习化学的兴趣,有利于调动学生的学习积极性.

练习册系列答案
相关题目
2. 甲醇是重要的化工原料,又可称为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
甲醇是重要的化工原料,又可称为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)═CH3OH(g)△H
②CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H2=-58kJ•mol-1
③CO2(g)+H2(g)═CO(g)+H2O(g)△H3=+41kJ•mol-1
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
则x=413;
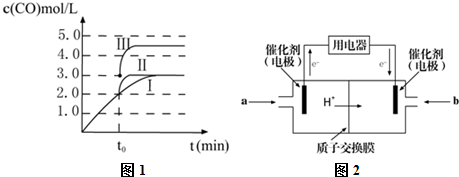
(2)若T℃时将6molCO2和8molH2充入2L密闭容器中发生反应②,测得H2的物质的量随时间变化关系如图中状态I(图中实线)所示.图中数据A(1,6)代表在1min时H2的物质的量是6mol.
①T℃时状态I条件下,0~3min内CH3OH的平均反应速率v=0.28mol/(L•min),平衡常数K=0.5;
②其他条件不变时,仅改变某一条件后测得H2的物质的量随时间变化如图中状态Ⅱ所示,则改变的条件可能是增大压强;
③其他条件不变,仅改变温度时,测得H2的物质的量随时间变化如图中状态Ⅲ所示,则状态Ⅲ对应的温度>(填“>”、“<”或“=”)T℃;
④若状态Ⅱ的平衡常数为K2,状态Ⅲ的平衡常数为K3,则K2>(填“>”、“<”或“=”)K3;
⑤一定温度下同,此反应在恒容容器中进行,能判断该反应达到化学平衡依据的是ac.
a.容器中压强不变 b.甲醇和水蒸汽的体积比保持不变
c.v正(H2)=3v逆(CH3OH) d.2个C═O断裂的同时有6个H-H断裂.
 甲醇是重要的化工原料,又可称为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
甲醇是重要的化工原料,又可称为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:①CO(g)+2H2(g)═CH3OH(g)△H
②CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H2=-58kJ•mol-1
③CO2(g)+H2(g)═CO(g)+H2O(g)△H3=+41kJ•mol-1
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 | H═H | C═O | C≡O | H-O | C-H |
| F/(kJ•mol-1) | 435 | 343 | 1076 | 465 | X |
(2)若T℃时将6molCO2和8molH2充入2L密闭容器中发生反应②,测得H2的物质的量随时间变化关系如图中状态I(图中实线)所示.图中数据A(1,6)代表在1min时H2的物质的量是6mol.
①T℃时状态I条件下,0~3min内CH3OH的平均反应速率v=0.28mol/(L•min),平衡常数K=0.5;
②其他条件不变时,仅改变某一条件后测得H2的物质的量随时间变化如图中状态Ⅱ所示,则改变的条件可能是增大压强;
③其他条件不变,仅改变温度时,测得H2的物质的量随时间变化如图中状态Ⅲ所示,则状态Ⅲ对应的温度>(填“>”、“<”或“=”)T℃;
④若状态Ⅱ的平衡常数为K2,状态Ⅲ的平衡常数为K3,则K2>(填“>”、“<”或“=”)K3;
⑤一定温度下同,此反应在恒容容器中进行,能判断该反应达到化学平衡依据的是ac.
a.容器中压强不变 b.甲醇和水蒸汽的体积比保持不变
c.v正(H2)=3v逆(CH3OH) d.2个C═O断裂的同时有6个H-H断裂.
6.甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成.已知:①将甲溶液分别与其它三种物质的溶液混合,均有白色沉淀生成;②0.1mol•L-1乙溶液中c(H+)>0.1mol•L-1;③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成.下列结论不正确的是( )
| A. | 甲溶液含有OH- | B. | 乙溶液含有SO42- | C. | 丙溶液含有Cl- | D. | 丁溶液含有Mg2+ |
3.反应3A(s)+3B(g)═2C(g)+D(g),经3min,B的浓度减少0.9mol•L-1.对此反应速率的表示正确的是( )
| A. | 用A表示的反应速率是0.4 mol•L-1•min-1 | |
| B. | 分别用B、C、D表示的反应速率之比是3:2:1 | |
| C. | 在2 min末的反应速率,用B表示是0.3 mol•L-1•min-1 | |
| D. | 在2 min内的反应速率,用C表示是0.3 mol•L-1•min-1 |
20.下列叙述正确的是( )
| A. | 1 L水中溶解了40 g NaOH后,所得溶液浓度为1 mol/L | |
| B. | 从1 L 2 mol/L的NaCl溶液中取出0.5 L,该溶液的浓度为1 mol/L | |
| C. | 将2.24 L(标准状况)HCl气体溶于水制成100 mL溶液,其物质的量浓度为1 mol/L | |
| D. | 配制1 L 0.2 mol/L的CuSO4溶液,需用32g胆矾 |