题目内容
12.25℃时,将VamLpH=1的硫酸溶液与VbmLpH=12的氢氧化钾溶液混合恰好呈中性,则Va:Vb=1:10.分析 混合溶液呈中性,则n(H+)=n(OH-),根据pH和氢离子的关系以及氢氧根离子浓度和氢离子、Kw之间的关系来计算即可.
解答 解:VamLpH=1的硫酸溶液与VbmLpH=12的氢氧化钾溶液混合恰好呈中性,则n(H+)=n(OH-),VamL×0.1mol/L=VbmL×$\frac{1{0}^{-14}}{1{0}^{-12}}$mol/L,解得Va:Vb=1:10.
故答案为:1:10.
点评 本题考查学生酸碱混合溶液pH的计算知识,属于综合知识的考查,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列说法错误的是( )
| A. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| B. | 放热反应和吸热反应决定于反应物的总能量与生成物的总能量的相对大小 | |
| C. | 已知:S(s)+O2(g)=SO2(g)△H1;S(g)+O2(g)=SO2(g)△H2;则△H1>△H2 | |
| D. | 凡经加热而发生的化学反应都是吸热反应 |
20.下列反应中,属于吸热反应的是( )
| A. | 氢氧化钠溶液与稀盐酸混合 | B. | 消石灰与氯化铵固体混合 | ||
| C. | 镁条与稀盐酸反应 | D. | 铝粉与氧化铁粉末共热 |
17.用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 0.1 mol/L稀硫酸中含有硫酸根数目为0.1NA | |
| B. | 9g H2O中含有H数目为1mol | |
| C. | 2.4g金属镁与足量的盐酸反应,生成氢分子数目为2NA | |
| D. | 1mol NH4+中含有电子数为10NA |
4.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2L的己烷所含的分子数为0.5NA | |
| B. | 28g乙烯在氧气中完全燃烧消耗氧气分子的数目为3NA | |
| C. | 1mol甲基(-CH3)所含的电子总数为10NA | |
| D. | 分子式为C2H6O中含有C-H(碳氢键)的数目为6NA |
2.下列物质属于芳香烃,但不是苯的同系物的是( )
①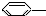 CH3 ②
CH3 ②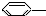 CH=CH2 ③
CH=CH2 ③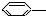 NO2
NO2
④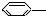 OH ⑤
OH ⑤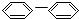 ⑥
⑥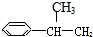
①
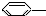 CH3 ②
CH3 ②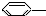 CH=CH2 ③
CH=CH2 ③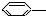 NO2
NO2④
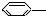 OH ⑤
OH ⑤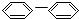 ⑥
⑥
| A. | ③④ | B. | ②⑤ | C. | ①②⑤⑥ | D. | ②③④⑤⑥ |
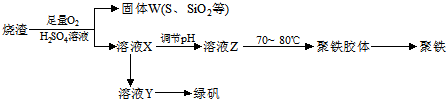
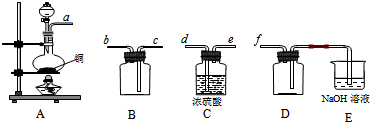
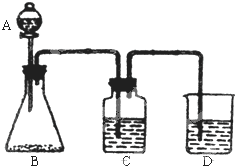 为了确定
为了确定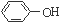 是一种弱酸,有人设计了如图所示的装置进行实验:
是一种弱酸,有人设计了如图所示的装置进行实验: .
.