题目内容
15.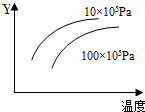 由可逆反应测绘出图象如下,纵坐标Y为生成物在平衡混合物中的体积百分含量,下列对该反应的判断正确的是( )
由可逆反应测绘出图象如下,纵坐标Y为生成物在平衡混合物中的体积百分含量,下列对该反应的判断正确的是( )| A. | 正反应为一定为放热反应 | B. | 逆反应为体积缩小的反应 | ||
| C. | 升高温度,平衡常数K值减小 | D. | 该反应在一定条件下可自发进行 |
分析 “定一议二”:温度不变时,增大压强,生成物的百分含量降低,说明平衡逆向移动,逆向为体积缩小方向,而题中未给出具体的可逆反应,但是可以确定生成物中一定有气体,压强不变时,升高温度,生成物的百分含量增大,说明平衡正向移动,正向为吸热反应.
解答 解:根据图示可以看出:压强不变,温度升高,产物的百分含量增大,所以平衡正向移动,反应是吸热的,温度不变,压强增大,产物的百分含量减小,所以平衡逆向移动,逆向为体积缩小方向.
A、正反应为吸热反应,故A错误;
B、逆向为体积缩小方向,故B正确;
C、正反应为吸热反应,升高温度,平衡常数K值增大,故C错误;
D、该反应是吸热的,但是不能确定焓变符号,所以无法判断反应在一定条件下是否自发,故D错误.
故选B.
点评 本题考查学生影响化学平衡移动的因素:温度、压强,注意“定一议二”法的应用,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.配制0.10mol/L乳酸钠(NaC3H5O3)溶液250mL,需用112g/L乳酸钠溶液的体积为( )
| A. | 50mL | B. | 40mL | C. | 25mL | D. | 15mL |
3.下列说法错误的是( )
| A. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| B. | 放热反应和吸热反应决定于反应物的总能量与生成物的总能量的相对大小 | |
| C. | 已知:S(s)+O2(g)=SO2(g)△H1;S(g)+O2(g)=SO2(g)△H2;则△H1>△H2 | |
| D. | 凡经加热而发生的化学反应都是吸热反应 |
10.写出下列物质的电离方程式:
KOHKOH═K++OH-
CuCl2CuCl2=Cu2++2Cl-
Fe2(SO4)3Fe2(SO4)3=2Fe3++3SO42-
Na2SNa2S=2Na++S2-.
KOHKOH═K++OH-
CuCl2CuCl2=Cu2++2Cl-
Fe2(SO4)3Fe2(SO4)3=2Fe3++3SO42-
Na2SNa2S=2Na++S2-.
20.下列反应中,属于吸热反应的是( )
| A. | 氢氧化钠溶液与稀盐酸混合 | B. | 消石灰与氯化铵固体混合 | ||
| C. | 镁条与稀盐酸反应 | D. | 铝粉与氧化铁粉末共热 |
4.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2L的己烷所含的分子数为0.5NA | |
| B. | 28g乙烯在氧气中完全燃烧消耗氧气分子的数目为3NA | |
| C. | 1mol甲基(-CH3)所含的电子总数为10NA | |
| D. | 分子式为C2H6O中含有C-H(碳氢键)的数目为6NA |
5.据某科学杂志报道,国外有一研究发现了一种新的球形分子,它的分子式为C60Si60,其分子结构好似中国传统工艺品“镂雕”,经测定其中包含C60,也有Si60的结构.下列叙述正确的是( )
| A. | 该物质有很高的熔点、很大的硬度 | |
| B. | 该物质形成的晶体属分子晶体 | |
| C. | 该物质分子中Si60被包裹在C60里面 | |
| D. | C60易溶于水 |
 的名称是2,5二甲基-3-乙基己烷.
的名称是2,5二甲基-3-乙基己烷.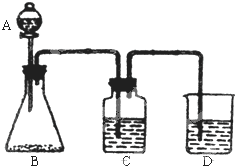 为了确定
为了确定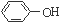 是一种弱酸,有人设计了如图所示的装置进行实验:
是一种弱酸,有人设计了如图所示的装置进行实验: