题目内容
19.“嫦娥三号”携带的“玉兔号”月球车使用的耐压外壳为钛合金.某种超高硬度钛合金含Ti、A1、V、Cr、Si等元素,该钛合金中硅元素在周期表中的位置为( )| A. | 第三周期ⅣA族 | B. | 第三周期ⅢA族 | C. | 第四周期ⅣA族 | D. | 第四周期ⅣB族 |
分析 主族元素中,原子核外电子层数与其周期数相等,最外层电子数与其族序数相等,据此判断Si元素在周期表中的位置.
解答 解:主族元素中,原子核外电子层数与其周期数相等,最外层电子数与其族序数相等,Si原子核外有3个电子层、最外层有4个电子,所以Si元素位于第三周期第IVA族,故选A.
点评 本题考查元素在周期表中位置判断,为高频考点,明确主族元素原子核外电子层数、最外层电子数与周期数、族序数之间的关系是解本题关键,熟悉前36号元素在周期表中的位置及原子结构,题目难度不大.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
9.下列物质之间的转化都一步能实现的是( )
| A. | Si→SiO2→H2SiO3→Na2SiO3 | |
| B. | Al→Al2O3→Al(OH)3→NaAlO2 | |
| C. | Na→Na2O→Na2O2→NaOH→Na2CO3→NaHCO3 | |
| D. | S→SO3→H2SO4→SO2→Na2SO3→Na2SO4 |
10.下列物质中,含有Cl-的是( )
①盐酸
②氯化钠溶液
③氯化钠固体
④次氯酸
⑤氯化氢气体.
①盐酸
②氯化钠溶液
③氯化钠固体
④次氯酸
⑤氯化氢气体.
| A. | ①②⑤ | B. | ①②③ | C. | ③④⑤ | D. | ②④⑤ |
14.在8NH3+3Cl2=N2+6NH4Cl反应中,有213g氯气参加了反应,则被氧化的NH3的物质的量是( )
| A. | 2mol | B. | 3mol | C. | 1.5mol | D. | 0.2mol |
4.标准状况下,均含有NA个电子的H2O和CH4,具有相同的( )
| A. | 物质的量 | B. | 体积 | C. | 质量 | D. | 氢原子数 |
11.影响物质体积大小的因素不包括( )
| A. | 物质的粒子数目 | B. | 粒子的大小 | C. | 粒子间的距离 | D. | 粒子的运动频率 |
8.证明溴乙烷中溴原子的存在,下列正确的操作步骤为( )
①加入AgNO3溶液 ②加入NaOH水溶液 ③加热
④加入蒸馏水 ⑤加稀硝酸至溶液呈酸性 ⑥加入NaOH醇溶液.
①加入AgNO3溶液 ②加入NaOH水溶液 ③加热
④加入蒸馏水 ⑤加稀硝酸至溶液呈酸性 ⑥加入NaOH醇溶液.
| A. | ④③①⑤ | B. | ③⑥⑤① | C. | ②③① | D. | ②③⑤① |
9.某羧酸脂的分子式为为C16H14O4,1mol该酯完全水解可得到2mol羧酸和1mol乙二醇(HOCH2-CH2OH),该羧酸的分子式为( )
| A. | C7H6O2 | B. | C8H8O4 | C. | C14H12O2 | D. | C6H6O4 |
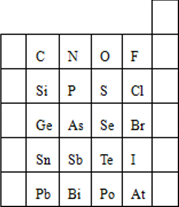 元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.