题目内容
8.证明溴乙烷中溴原子的存在,下列正确的操作步骤为( )①加入AgNO3溶液 ②加入NaOH水溶液 ③加热
④加入蒸馏水 ⑤加稀硝酸至溶液呈酸性 ⑥加入NaOH醇溶液.
| A. | ④③①⑤ | B. | ③⑥⑤① | C. | ②③① | D. | ②③⑤① |
分析 检验溴乙烷中溴元素,应在碱性条件下加热水解或碱性醇溶液条件下发生消去,最后加入硝酸酸化,加入硝酸银,观察是否有黄色沉淀生成.
解答 解:证明溴乙烷中溴元素的存在,先发生②加入氢氧化钠溶液并③加热,发生水解反应生成NaBr,
再发生⑤加入稀硝酸至溶液呈酸性,
最后①加入硝酸银溶液,生成淡黄色沉淀,则证明含溴元素,
即操作顺序为②③⑤①,
故选D.
点评 本题考查溴乙烷的性质,题目难度不大,易错点为卤代烃水解是碱性溶液中进行,加硝酸银时必须先加酸中和碱才能出现溴化银沉淀,注意实验的操作步骤.

练习册系列答案
相关题目
18.在一种酸性溶液中存在NO3-、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,由此可推知该溶液中( )
| A. | 一定含有I-,不能确定是否含有Cl- | B. | 一定含有NO3- | ||
| C. | 不含有Fe3+,可能含有NO3- | D. | 一定含有I-、NO3-和Cl- |
19.“嫦娥三号”携带的“玉兔号”月球车使用的耐压外壳为钛合金.某种超高硬度钛合金含Ti、A1、V、Cr、Si等元素,该钛合金中硅元素在周期表中的位置为( )
| A. | 第三周期ⅣA族 | B. | 第三周期ⅢA族 | C. | 第四周期ⅣA族 | D. | 第四周期ⅣB族 |
16.X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )
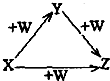
①C、CO ②Fe、Fe(NO3)2 ③Na2CO3、NaHCO3.

①C、CO ②Fe、Fe(NO3)2 ③Na2CO3、NaHCO3.
| A. | ①②③ | B. | ①② | C. | ③④ | D. | ①③ |
3.如表实验操作正确且能达到预期目的是( )
| 实验目的 | 实验操作 | |
| A | 比较水和乙醇中羟基氢的活泼性强弱 | 用等量的金属钠分别与水和乙醇反应 |
| B | 检验溴乙烷中含有溴元素 | 先加NaOH溶液共热,然后加入AgNO3溶液 |
| C | 证明CH2=CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液 |
| D | 除去苯中的少量苯酚 | 加入过量浓溴水,振荡后过滤 |
| A. | A | B. | B | C. | C | D. | D |
13.不能够用于鉴别SO2和CO2两种无色气体的溶液是( )
| A. | 品红溶液 | B. | 酸性高锰酸钾溶液 | ||
| C. | 氢硫酸溶液 | D. | 澄清石灰水 |
20.常见的有机反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤加聚 ⑥水解 ⑦还原.其中能在有机化合物中引入-OH的反应类型有( )
| A. | ①②③④⑤⑥ | B. | ③④⑤⑥ | C. | ②③④⑤ | D. | ②⑥⑦ |
17.下列各组物质中,化学键类型相同,化合物类型也相同的是( )
| A. | SO2 Na2SO4 | B. | CH4 H2O | C. | KCl HCl | D. | NaOH Cl2 |
18.下列关于元素原子或离子半径的比较.正确的是( )
| A. | r(Al)>r(Si)>r(C)>r(N) | B. | r(Na+)<r(Mg2+)<r(Al3+)<r(F-) | ||
| C. | r(K+)>r(Ca2+)>r(S2-)>r(Cl-) | D. | r(N)<r(S)<r(O)<r(P) |