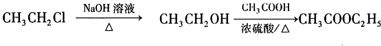题目内容
3.有50L的CO和CO2的混合气体,其气体密度是相同条件下H2密度的19倍.则:(1)混合气体中CO和CO2的体积比为多少?
(2)CO和CO2的分别占有的体积为多少?
分析 (1)CO和CO2混合气体的密度是相同条件下H2密度的19倍,所以混合气体的平均相对分子质量是19×2=32,设混合物中CO和CO2物质的量分别为xmol、ymol,根据相对分子质量求混合物中CO和CO2物质的量之比,相同条件下气体体积之比等于物质的量之比;
(2)根据总体积50L及(1)中的体积之比计算出一氧化碳和二氧化碳的体积.
解答 解:(1)CO和CO2混合气体的密度是相同条件下H2密度的19倍,所以混合气体的平均相对分子质量是19×2=32,设混合物中CO和CO2物质的量分别为xmol、ymol,
则:$\frac{28x+44y}{x+y}$=32,整理可得x:y=3:1,
相同条件下气体体积之比等于物质的量之比,所以混合气体中CO和CO2的体积比为3:1,
答:混合气体中CO和CO2的体积比为3:1;
(2)混合气体体积为50L,混合气体中CO和CO2的体积比为3:1,则混合气体中CO的体积为:50L×$\frac{3}{1+3}$=37.5L,CO2的体积为:50L-37.5L=12.5L,
答:CO和CO2所占有的体积分别为37.5L、12.5L.
点评 本题考查了物质的量的计算,题目难度不大,明确相对分子质量与相对密度的关系为解答关键,试题侧重考查学生的分析能力及化学计算能力.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
14.设nA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,6.72L NO2与水充分反应转移的电子数目为0.2nA | |
| B. | 1mol的羟基与1 mol的氢氧根离子所含电子数均为9nA | |
| C. | 标准状况下,22.4L盐酸含有nA个HCl分子 | |
| D. | 1L1mol•L-1的NaClO 溶液中含有ClO-的数目为nA |
11.100mL 6mol•L-1 H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量( )
| A. | 碳酸钠溶液 | B. | 氢氧化钠溶液 | C. | 硫酸钾溶液 | D. | 硝酸钠溶液 |
18.一定条件下,在容积固定的某密闭容器中发生反应N2+3H2?2NH3.在10s内N2的浓度由5mol/L降至4mol/L,下列说法正确的是( )
| A. | 用NH3表示的化学反应速率为0.1 mol/(L•s) | |
| B. | 反应足够长时间,N2、H2中至少有一种物质浓度降为零 | |
| C. | 增加H2的浓度或降低温度都会加快该反应的速率 | |
| D. | 使用合适的催化剂,可以加快该反应的速率 |
15.在日常生活中,下列做法错误的是( )
| A. | 用灼烧法鉴别毛织品和棉织品 | |
| B. | 用纯碱洗涤锅盖上的油渍 | |
| C. | 用将铁屑、溴水、苯混合制溴苯 | |
| D. | 用淀粉溶液鉴别加碘食盐和不含碘的食盐 |
12.关于阿佛加德罗常数NA的叙述中,正确的是( )
| A. | 10 g H218O中所含的中子数为5NA | |
| B. | 1 mol 铁单质与足量的硫单质充分反应,电子转移数目为3NA | |
| C. | 在1 L 0.1mol/L的NH4Cl溶液中,阴、阳离子总数小于0.2NA | |
| D. | 一定条件下,将1mol N2和3mol H2充分反应,产物分子数目小于2NA |
13.钢铁防腐方法有许多种,如图是其中的一种方法,描述正确的是( )
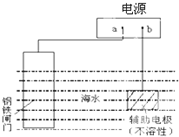

| A. | 图所示是牺牲阳极阴极保护法 | |
| B. | a为电源正极 | |
| C. | 电子流向:a→铁闸门,辅助电极→b | |
| D. | 辅助电极上的反应:O2+2H2O+4e→4OH- |
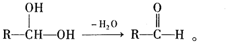
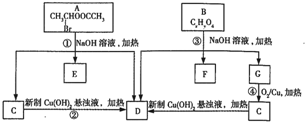



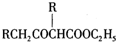 +C2H3OH,请以G为唯一有机试剂合成乙酸乙酯(CH3OCH2COOC2H3),设计合成路线(其他试剂任选),合成路线流程图示例:
+C2H3OH,请以G为唯一有机试剂合成乙酸乙酯(CH3OCH2COOC2H3),设计合成路线(其他试剂任选),合成路线流程图示例: