题目内容
17.在第ⅦA族元素的卤化氢中,最容易分解成单质的是( )| A. | HI | B. | HBr | C. | HCl | D. | HF |
分析 同主族自上而下得电子能力减弱,非金属性减弱,非金属性越强氢化物越稳定,F、Cl、Br、I为第ⅦA族元素,且从上到下排列,以此来解答.
解答 解:同主族自上而下电子层增多,原子半径增大,原子核对最最外层电子的吸引减弱,金属性增强、非金属性减弱,F、Cl、Br、I均位于元素周期表中第ⅦA族元素,且从上到下排列,从上向下非金属性减弱,则F的非金属性最强,所以其气态氢化物最稳定,I的非金属性弱,HI易分解成单质,
故选A.
点评 本题考查元素性质在周期表中的递变规律,熟悉第ⅦA族元素非金属性的变化规律及气态氢化物的稳定性的比较方法即可解答,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.决定化学反应速率的主要因素是( )
| A. | 温度和压强 | B. | 催化剂 | ||
| C. | 参加反应物质的性质 | D. | 各反应物和生成物的浓度 |
2.据报道合成和分离了含高能量的N5+的化合物N5AsF6,下列叙述错误的是( )
| A. | N5+具有34个电子 | B. | N5+中氮-氮之间是以共价键结合 | ||
| C. | 化合物N5AsF6中As的化合价为+1 | D. | 化合物N5AsF6中F的化合价为-1 |
9.下列反应属于吸热反应的是( )
| A. | 锌粒与稀硫酸的反应 | |
| B. | 生石灰与水的反应 | |
| C. | 甲烷在空气中燃烧的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
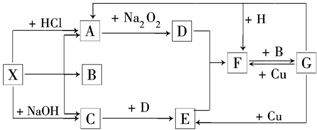


 .
. 同分异构体有4种.
同分异构体有4种. 的合成路线(用流程图表示,无机试剂任选)注:合成路线的书写格式参照如下实例:
的合成路线(用流程图表示,无机试剂任选)注:合成路线的书写格式参照如下实例: