题目内容
4.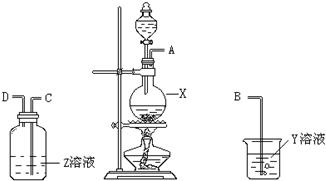 某化学课外兴趣小组为探究铜与浓硫酸反应产物的性质,拟用如图所示的装置进行实验.
某化学课外兴趣小组为探究铜与浓硫酸反应产物的性质,拟用如图所示的装置进行实验.请回答下列问题:
(1)仪器X的名称为:圆底烧瓶,Z溶液为:品红
(2)实验装置连接顺序应为:A接C,D接B;
(3)若Y为足量的氢氧化钠,则烧杯中发生反应的化学方程式为:2NaOH+SO2=Na2SO3+H2O
(4)写出铜与浓硫酸反应的化学方程式:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
分析 (1)根据仪器X的特点确定名称;二氧化硫能使品红褪色;
(2)实验装置连接顺序应为:先是制备装置,再是检验装置,最后进行尾气处理;
(3)Y为足量的氢氧化钠,二氧化硫属于酸性气体,二者之间反应得到盐和水;
(4)铜与浓硫酸在加热条件下反应生成硫酸铜和水、二氧化硫.
解答 解:(1)仪器X的名称为圆底烧瓶,二氧化硫能使品红褪色,Z溶液为品红,故答案为:圆底烧瓶;品红;
(2)实验装置连接顺序应为:先是制备装置,再是检验装置,最后进行尾气处理,即A接C,再接D,故答案为:C;D;
(3)Y为足量的氢氧化钠,二氧化硫属于酸性气体,则烧杯中发生反应的化学方程式为:2NaOH+SO2=Na2SO3+H2O,故答案为:2NaOH+SO2=Na2SO3+H2O;
(4)铜与浓硫酸在加热条件下反应生成硫酸铜和水、二氧化硫,即Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
点评 本题考查了铜和浓硫酸的反应,熟悉浓硫酸、二氧化硫的性质是解题关键,题目难度不大.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
8.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 1 mol羟基与1 mol氢氧根离子所含的电子数均为9NA | |
| B. | 常温下,44 g N2O和CO2组成的混合气体,所含原子数为3NA | |
| C. | 0.1 mol/L的NaClO溶液,含有的阴离子数为0.1NA | |
| D. | 常温下,将 1 mol Fe投入过量浓硝酸中,转移的电子数为3NA |
9.现要配置一定物质的量浓度的100mL1mol•L-1NaOH溶液,下列操作正确的是( )
| A. | 在托盘天平的两个托盘上各放一张大小一样的纸,然后将NaOH固体放在纸上进行称量 | |
| B. | 把称量的NaOH固体放入盛有适量蒸馏水的烧杯中,溶解后立即把溶液转移到容量瓶中 | |
| C. | 用蒸馏水洗涤烧杯、玻璃棒2~3次,每次洗涤后的溶液都注入容量瓶中 | |
| D. | 沿着玻璃棒往容量瓶中加入蒸馏水,直到溶液凹液面恰好与刻度相切 |
14.如表是稀硫酸与某金属反应的实验数据:
分析上述数据,回答下列问题:
(1)实验4和5表明,固体反应物的表面积对反应速率有影响,固体表面积越大反应速率越快,能表明同一规律的实验还有1和2(填实验序号);
(2)实验1、3、4、6、8表明反应物浓度对反应速率产生影响,能表明同一规律的实验还有2和5(填实验序号);
(3)本实验中影响反应速率的其他因素还有反应温度,其实验序号是6和7,8和9.
(4)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因:可能是反应物硫酸过量,金属用量相同,放出的热量相同.
| 实验序号 | 金属质量 | 金属状态 | c(H2SO4)/mol•L-1 | V(H2SO4)/mL | 溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 丝 | 1.1 | 50 | 30 | 44 | 40 |
(1)实验4和5表明,固体反应物的表面积对反应速率有影响,固体表面积越大反应速率越快,能表明同一规律的实验还有1和2(填实验序号);
(2)实验1、3、4、6、8表明反应物浓度对反应速率产生影响,能表明同一规律的实验还有2和5(填实验序号);
(3)本实验中影响反应速率的其他因素还有反应温度,其实验序号是6和7,8和9.
(4)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因:可能是反应物硫酸过量,金属用量相同,放出的热量相同.
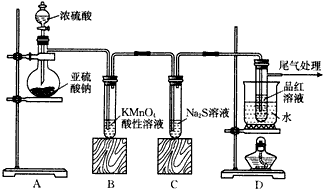
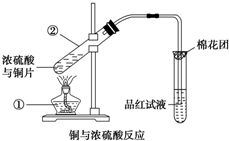 如图是铜与浓硫酸反应的实验装置图,请回答下列问题.
如图是铜与浓硫酸反应的实验装置图,请回答下列问题.