题目内容
13.一定温度下将6mol A及6mol B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)═xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60%,C的平均反应速率是0.36mol/(L•min).求:(1)平衡时D的浓度=1.2mol/L.
(2)B的平均反应速率υ(B)=0.12mol/(L.min).
(3)x=3.
(4)开始时容器中的压强与平衡时的压强之比为10:11(化为最简整数比).
分析 3A(g)+B(g)?xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60%,则
3A(g)+B(g)?xC(g)+2D(g),
开始(mol/L) 3 3 0 0
转化 3×60% 0.6 1.2
平衡 1.2 2.4 0.6x 1.2
(1)由上述分析可知平衡状态D的浓度;
(2)结合v=$\frac{△c}{△t}$计算;
(3)结合速率之比等于化学计量数之比计算;
(4)开始时容器中的压强与平衡时的压强之比等于反应前后的物质的量之和的比.
解答 解:3A(g)+B(g)?xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60%,则
3A(g)+B(g)?xC(g)+2D(g),
开始(mol/L) 3 3 0 0
转化 3×60% 0.6 1.2
平衡 1.2 2.4 0.6x 1.2
(1)由上述分析可知平衡状态D的浓度为1.2mol/L,故答案为:1.2mol/L;
(2)B的平均反应速率υ(B)=$\frac{0.6mol/L}{5min}$=0.12mol/( L.min),故答案为:0.12mol/( L.min)
(3)由速率之比等于化学计量数之比可知,$\frac{1}{x}$=$\frac{0.12}{0.36}$,解得x=3,故答案为:3;
(4)开始时容器中的压强与平衡时的压强之比等于反应前后的物质的量之和的比,为(6+6)mol:(1.2+2.4+0.6×3+1.2)mol/L×2L=10:11,
故答案为:10:11.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法计算、速率及压强比的计算方法为解答的关键,侧重分析与计算能力的考查,题目难度不大.

 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案| A. | 电解质 | B. | 氧化剂 | C. | 还原剂 | D. | 胶体 |
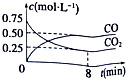 一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g)△H>0,1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示.
一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g)△H>0,1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示.(1)该反应的平衡常数表达式K=$\frac{c(CO)}{c(C{O}_{2})}$.
(2)下列措施中能使平衡时K增大的是B(填序号).
A.升高温度B.增大压强C.充入一定量COD.降低温度
(3)8分钟内,CO2的平均反应速率v(CO2)=0.0625mol•L-1•min-1.
(4)1100℃时,2L的密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 |
| 反应物投入量 | 3mol Fe、 2mol CO2 | 4mol FeO、 3mol CO |
| CO的浓度(mol•L-1) | c1 | c2 |
| CO2的体积分数 | φ1 | φ2 |
| 体系压强(Pa) | p1 | p2 |
| 气态反应物的转化率 | α1 | α2 |
A.p1<p2 B.φ1=φ2 C.2c1=3c2 D.α1=α2
②求c1=0.67mol•L-1、α2=33.3%.
发生的化学反应为:2NH3(g)+NO(g)+NO2(g)$?_{催化剂}^{180℃}$2N2(g)+3H2O(g) 正反应放热在恒容的密闭容器中,下列有关说法正确的是( )
| A. | 平衡时,其他条件不变,升高温度平衡正向移动 | |
| B. | 平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 | |
| C. | 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 | |
| D. | 单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡 |
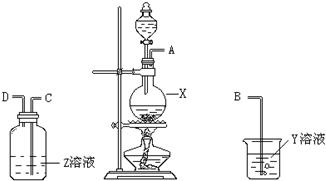 某化学课外兴趣小组为探究铜与浓硫酸反应产物的性质,拟用如图所示的装置进行实验.
某化学课外兴趣小组为探究铜与浓硫酸反应产物的性质,拟用如图所示的装置进行实验.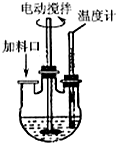 实验室制取高纯NaI晶体(无色)可按下列步骤进行:按化学计量称取各原料,在三颈烧瓶中(如图)先加入适量的高纯水,然后按Na2CO3、I2和水合肼的投料顺序分批加入.
实验室制取高纯NaI晶体(无色)可按下列步骤进行:按化学计量称取各原料,在三颈烧瓶中(如图)先加入适量的高纯水,然后按Na2CO3、I2和水合肼的投料顺序分批加入.