题目内容
12.鉴别苯酚溶液、己烷、己烯、乙酸溶液和乙醇液体,可选用的最佳试剂是( )| A. | 溴水、Cu(OH)2 | B. | FeCl3溶液、金属钠、溴水、石蕊试液 | ||
| C. | 石蕊试液、溴水 | D. | KMnO4酸性溶液、石蕊试液 |
分析 A.氢氧化铜需要新制;
B.操作繁琐;
C.试剂易得,现象明显;
D.石蕊可检验乙酸,高锰酸钾不能鉴别苯酚、己烯、乙醇.
解答 解:D中不能鉴别;A、B、C选项中试剂均可鉴别上述物质,但A需新制Cu(OH)2;若用B选项中试剂来鉴别其操作步骤较繁琐,只有C中用石蕊可鉴别出乙酸溶液,用FeCl3溶液可鉴别出苯酚溶液,用溴水可鉴别出己烯,余下的乙醇和己烷可用金属钠鉴别,则C选项中试剂则操作简捷,现象明显,符合“鉴别液体最佳试剂”,
故选C.
点评 本题考查有机物的鉴别,为高频考点,把握有机物的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意最佳试剂的选择,题目难度不大.

练习册系列答案
相关题目
20. 2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品.
2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品.
(1)NaCN溶液中各离子浓度大小关系为c(Na+)>c(CN-)>c(OH-)>c(H+).
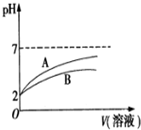
已知NaCN遇酸能产生HCN;25℃时,HCN的电离常数Ka=6.2×10-10 mol•L-1;CH3COOH的电离常数Ka=1.7×10-5 mol•L-1.体积均为100mL、pH=2的CH3COOH溶液和HCN溶液,加水稀释过程中溶液的pH变化与溶液体积的关系如图所示,则表示CH3COOH溶的pH变化趋势的曲线是A(选填“A”或“B”);相同条件下,NaCN溶液的pH>(选填“>”、“=”或“<”)CH3COONa溶液的pH.
(2)200℃固体硝酸铵可以分解为N2O和H2O,此过程中每转移电子8mol放出热量84.8kJ,写出此反应的热化学方程式NH4NO3(s)=N2O(g)+2H2O(g)△H=-42.4 kJ•mol-1.
(3)工业上用氯气和二氧化钛制备TiCl4,一定条件下发生反应:
TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g);△H>0.此温度下,该反应的平衡常数为400,在密闭容器中加入TiO2(s)和Cl2(g),反应到t时刻测得各组分的浓度如表所示:
①根据表中数据判断t时刻此反应向正反应方向进行(选填“正”或“逆”).
②若经10min反应达到平衡,则该时间内反应速率v(Cl2)=0.16mol•L-1•min-1;下列措施中,可以使平衡向右移动的是d(选填序号).
a.使用催化剂b.增大压强c.减小压强d.升高温度.
 2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品.
2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品.(1)NaCN溶液中各离子浓度大小关系为c(Na+)>c(CN-)>c(OH-)>c(H+).
已知NaCN遇酸能产生HCN;25℃时,HCN的电离常数Ka=6.2×10-10 mol•L-1;CH3COOH的电离常数Ka=1.7×10-5 mol•L-1.体积均为100mL、pH=2的CH3COOH溶液和HCN溶液,加水稀释过程中溶液的pH变化与溶液体积的关系如图所示,则表示CH3COOH溶的pH变化趋势的曲线是A(选填“A”或“B”);相同条件下,NaCN溶液的pH>(选填“>”、“=”或“<”)CH3COONa溶液的pH.
(2)200℃固体硝酸铵可以分解为N2O和H2O,此过程中每转移电子8mol放出热量84.8kJ,写出此反应的热化学方程式NH4NO3(s)=N2O(g)+2H2O(g)△H=-42.4 kJ•mol-1.
(3)工业上用氯气和二氧化钛制备TiCl4,一定条件下发生反应:
TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g);△H>0.此温度下,该反应的平衡常数为400,在密闭容器中加入TiO2(s)和Cl2(g),反应到t时刻测得各组分的浓度如表所示:
| 物质 | Cl2 | TiCl4 | O2 |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
②若经10min反应达到平衡,则该时间内反应速率v(Cl2)=0.16mol•L-1•min-1;下列措施中,可以使平衡向右移动的是d(选填序号).
a.使用催化剂b.增大压强c.减小压强d.升高温度.
17.某元素X的最高价氧化物对应的水化物的化学式为HnXO2n-2,则在其气态氢化物中,X的化合价为( )
| A. | -(12-3n) | B. | -(12-5n) | C. | -(6-3n) | D. | -(10-n) |
4.下列各组物质不属于同素异形体的是( )
| A. | CO、CO2 | B. | O2、O3 | C. | 红磷、白磷 | D. | 金刚石、石墨 |
1.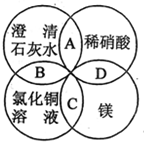 镁、稀硝酸、澄清石灰水、氯化铜溶液是中学化学中的常见物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )
镁、稀硝酸、澄清石灰水、氯化铜溶液是中学化学中的常见物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )
 镁、稀硝酸、澄清石灰水、氯化铜溶液是中学化学中的常见物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )
镁、稀硝酸、澄清石灰水、氯化铜溶液是中学化学中的常见物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )| A. | OH-+HNO3═H2O+NO3- | B. | Ca(OH)2+Cu2+═Ca2++Cu(OH)2 | ||
| C. | Mg+Cu2+═Cu+Mg2+ | D. | Mg+2H+=Mg2++H2↑ |
2.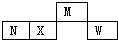 短周期主族元素M、N、X、W在元素周期表中的相对位置如图所示,N元素的单质常用作半导体材料.下列判断正确的是( )
短周期主族元素M、N、X、W在元素周期表中的相对位置如图所示,N元素的单质常用作半导体材料.下列判断正确的是( )
 短周期主族元素M、N、X、W在元素周期表中的相对位置如图所示,N元素的单质常用作半导体材料.下列判断正确的是( )
短周期主族元素M、N、X、W在元素周期表中的相对位置如图所示,N元素的单质常用作半导体材料.下列判断正确的是( )| A. | 原子半径的大小:W>X>M | |
| B. | 气态氢化物的稳定性:N>X>M | |
| C. | 对应的含氧酸的酸性强弱:W>X>N | |
| D. | W分别与N、X形成的化合物中的化学键均为极性键 |
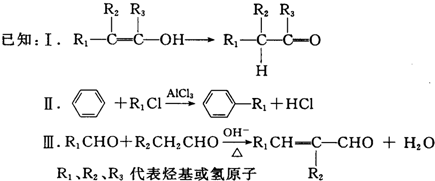
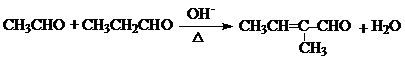 .
.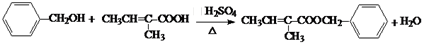 .
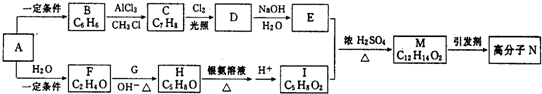
. 为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应.乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去,再与溴水反应.请你回答下列问题:
为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应.乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去,再与溴水反应.请你回答下列问题: