题目内容
9.A、B、C、D四种短周期元素,其中A、B同周期,A、C同主族,原子半径D>C>A>B.C原子核内质子数等于A、B原子电子数之和,C原子最外层电子数是D原子最外层电子数的4倍.试回答:(1)写出元素名称:A碳,D钠
(2)B在元素周期表中的位置第二周期第ⅥA族.
(3)A、B、C的最简单氢化物的稳定性由强到弱的顺序是H2O>CH4>SiH4(填化学式).
(4)A与B形成的三原子分子甲的电子式是
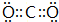 ,B与D形成的原子个数比为1:1的化合物乙的电子式是
,B与D形成的原子个数比为1:1的化合物乙的电子式是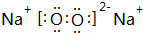 .
.(5)甲和乙反应的化学方程式是2CO2+2Na2O2═2Na2CO3+O2.
分析 A、B、C、D四种短周期元素,根据原子半径D>C>A>B,且A、B同周期,A、C同主族,推知A、B、C、D在周期表中的大致相对位置为: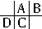 ,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的4倍,则D最外层电子数只能为1,故D为钠,C为硅,A为碳,据此解答.
,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的4倍,则D最外层电子数只能为1,故D为钠,C为硅,A为碳,据此解答.
解答 解:A、B、C、D四种短周期元素,根据原子半径D>C>A>B,且A、B同周期,A、C同主族,推知A、B、C、D在周期表中的大致相对位置为: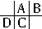 ,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的4倍,则D最外层电子数只能为1,故D为钠,C为硅,A为碳.
,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的4倍,则D最外层电子数只能为1,故D为钠,C为硅,A为碳.
(1)由上述分析可知,A为碳,D为钠,故答案为:碳;钠;
(2)B为O元素,处于周期表中第二周期第ⅥA族,故答案为:第二周期第ⅥA族;
(3)非金属性O>C>Si,故氢化物稳定性H2O>CH4>SiH4,故答案为:H2O>CH4>SiH4;
(4)A与B形成的三原子分子甲为CO2,电子式是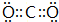 ,B与D形成的原子个数比为1:1的化合物乙是Na2O2,电子式是
,B与D形成的原子个数比为1:1的化合物乙是Na2O2,电子式是 ,
,
故答案为: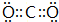 ;
; ;
;
(5)二氧化碳与过氧化钠反应生成碳酸钠与氧气,反应方程式为:2CO2+2Na2O2═2Na2CO3+O2,故答案为:2CO2+2Na2O2═2Na2CO3+O2.
点评 本题考查元素位置结构性质的关系应用,题目难度中等,本题的关键是正确推断元素的种类,确定其在周期表中的相对位置.

练习册系列答案
相关题目
19.放射性同位素${\;}_{92}^{238}$U的原子核内的中子数和核外电子数之差是( )
| A. | 54 | B. | 92 | C. | 146 | D. | 238 |
20.下列鉴别方法不可行的是( )
| A. | 用KMnO4(H+)溶液鉴别甲苯、丙烯、已烷 | |
| B. | 用溴水鉴别苯、丙烯、四氯化碳 | |
| C. | 用水鉴别乙醇、苯、四氯化碳 | |
| D. | 用NaOH溶液鉴别溴乙烷、甲苯、硝基苯 |
14.下列各组物质中,两者互为同分异构体的是( )
①异丁烷和新戊烷 ②NH4CNO和CO(NH2)2
③C2H5NO2和NH2CH2COOH ④2,3-二甲基戊烷和2,2,3-三甲基丁烷.
①异丁烷和新戊烷 ②NH4CNO和CO(NH2)2
③C2H5NO2和NH2CH2COOH ④2,3-二甲基戊烷和2,2,3-三甲基丁烷.
| A. | ①②③ | B. | ②③④ | C. | ②③ | D. | ③④ |
18.下列微粒中,与NH4+的电子总数和质子总数都相同的是( )
| A. | Na+ | B. | F | C. | OH- | D. | CH4 |
19.下列化合物在一定条件下,既能发生消去反应又能发生水解反应的是( )
| A. | CH3Cl | B. | 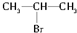 | C. | 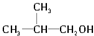 | D. | 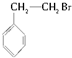 |
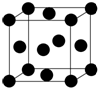 铁和铜都是日常生活中常见的金属,有着广泛的用途.请回答下列问题:
铁和铜都是日常生活中常见的金属,有着广泛的用途.请回答下列问题: