题目内容
4.下列有关氢化物的叙述中正确的( )| A. | 气态氢化物稳定性:PH3>CH4 | |
| B. | HCl的电子式为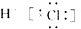 | |
| C. | D2O分子所有原子均达到最外层8e-稳定结构 | |
| D. | VIIA族元素中F的最高价氧化物对应水化物酸性最强 |
分析 A.元素非金属性越强,氢化物越稳定;
B.HCl为共价化合物,不含离子键;
C.D原子的最外层达到2e-稳定结构;
D.F的电负性最强,没有正化合价.
解答 解:A.由于非金属性P>C,所以气态氢化物稳定性:PH3>CH4,故A正确;
B.HCl分子是由1个氢原子和1个氯原子通过共用1对电子结合而成的共价化合物其电子式为 ,故B错误;
,故B错误;
C.D原子的最外层达到2e-稳定结构,O原子达到了最外层8e-稳定结构,故C错误;
D.F的电负性最强,没有正化合价,VIIA族元素中Cl的最高价氧化物对应水化物酸性最强,故D错误;
故选A.
点评 本题考查了元素周期律,难度不大,涉及非金属性的判断、原子结构、电子式的书写等知识,难度不大,注意酸性最强的是高氯酸.

练习册系列答案
相关题目
11.下列说法中正确的是( )
| A. | 闻名世界的中国陶瓷、酿酒、造纸技术都充分应用了化学工艺 | |
| B. | 植物油和矿物油都是碳氢化合物 | |
| C. | 光导纤维维、合成纤维和玻璃纤维都是新型无机非金属材料 | |
| D. | 蛋白质的水解和油脂的皂化都是由高分子生成小分子的过程 |
15.下列化学用语书写正确的是( )
| A. | 氯原子的结构示意图: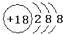 | |
| B. | HClO的结构式为:H-Cl-O | |
| C. | 氯化镁的电子式: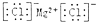 | |
| D. | 用电子式表示氯化氢分子的形成过程:H•+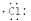 →H+ →H+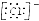 |
12.下列说法正确的是( )
| A. | 常温下可用铁制容器来盛装浓硫酸、说明常温下铁与浓硫酸不反应 | |
| B. | 同一元素的各种同位素的物理性质不同、化学性质相同 | |
| C. | 金属元素的原子只有还原性,离子只有氧化性 | |
| D. | 取碘水于试管中,加入汽油振荡后静置,其现象为下层呈紫红色 |
19.放射性同位素${\;}_{92}^{238}$U的原子核内的中子数和核外电子数之差是( )
| A. | 54 | B. | 92 | C. | 146 | D. | 238 |
16.NA为阿伏加罗常数,下列有关说法正确的是( )
| A. | 16.5克过氧化钾晶体中,含0.3NA个阴离子 | |
| B. | 1mol铜粉与硫粉充分反应可转移2mol电子 | |
| C. | 含等物质的量溶质的NaHSO4溶液和Na2SO4 溶液中,均含2NA个阳离子 | |
| D. | 20 g NH3T+中含有中子数为9NA |
13.下列描述中正确的是( )
| A. | CS2为V形的极性分子 | |
| B. | ClO3-的空间构型为三角锥形 | |
| C. | BF3是三角锥形分子 | |
| D. | SiF4和SO32-的中心原子均为sp2杂化 |
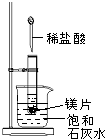 如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答下列问题:
如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答下列问题: