题目内容
10.某学生中和滴定实验的过程如下:(1)取一支碱式滴定管;(2)用蒸馏水洗净;(3)即加入待测的NaOH溶液;(4)记录液面刻度读数;(5)用酸式滴定管精确放出一定量标准酸液;(6)置于未经标准酸液润洗的洁净的锥形瓶中;(7)加入适量蒸馏水;(8)加入酚酞试液两滴;(9)滴定时,边滴边振荡;(10)边注视滴定管内液面的变化;(11)当小心滴到溶液由无色变为粉红色时,即停止滴定;(12)记录液面刻度读数;(13)根据滴定管的两次读数得出NaOH溶液体积为22mL,指出上述实验过程中错误之处(用序号表示)(3)、(10)、(11)、(13).分析 滴定操作时,滴定管必须使用待装液润洗,锥形瓶不能润洗;滴定时眼睛应该注视锥形瓶中混合液颜色变化;滴定终点现象为溶液由无色变成粉红色且半分钟不褪色;滴定管读数应该读到0.01mL.
解答 解:(3)加入待测的NaOH溶液,碱式滴定管用蒸馏水洗完,必须使用待装液润洗,才能量取氢氧化钠溶液,故(3)错误;
(10)边注视滴定管内液面变化,该操作错误,滴定时眼睛应该注视锥形瓶中溶液颜色变化,以便及时判断达到终点,故(10)错误;
(11)当小心滴到溶液由无色变成粉红色且半分钟不褪色时,才能停止滴定,否则提前结束滴定,影响滴定结果,故(11)错误;
(13)滴定管准确度为0.01mL,滴定管的两次读数得出NaOH溶液的体积应该为22.00mL,故(13)错误;
故答案为:(3)、(10)、(11)、(13).
点评 本题考查化学实验方案的评价,主要考查氧化还原滴定的操作、仪器、误差分析,难度不大,注意实验的基本操作方法及其规范性和注意事项,注意:滴定时眼睛注视锥形瓶内液体颜色变化而不是滴定管内液面变化,为易错点.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
19.在298K和101KPa时,2N2O5(g)=4NO2(g)+O2(g);△H=+56.7kJ/mol,能自发进行的合理解释是( )
| A. | 是熵减反应 | B. | 是熵增效应大于能量效应 | ||
| C. | 是吸热反应 | D. | 是放热反应 |
18.将A和B加入密闭容器中,在一定条件下发生反应:A(g)+B(s)?2C(g)△H,忽略固体体积,平衡时C的体积分数(%)随温度和压强的变化如下表所示.据表回答:
(1)该反应的△H>0(填“>”或“<”).
(2)a、b、e、f的大小顺序是e>f>a>b.
(3)平衡常数的大小关系是K(700℃)<K(950℃)(填“>”或“<”).
(4)850℃、4.0MPa时A的转化率为60%.
| 压强/MPa 体积分数/% 温度/℃ | 2.0 | 4.0 | 6.0 |
| 700 | 55.0 | a | b |
| 850 | c | 75.0 | d |
| 950 | e | f | 85.0 |
(2)a、b、e、f的大小顺序是e>f>a>b.
(3)平衡常数的大小关系是K(700℃)<K(950℃)(填“>”或“<”).
(4)850℃、4.0MPa时A的转化率为60%.
5.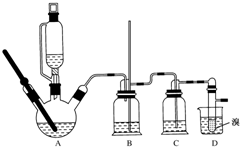 用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
有关数据列表如下:
回答下列问题:
(1)有乙醇制备1,2-二溴乙烷的两个方程式:CH3CH2OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O、CH2=CH2+Br-Br→CH2Br-CH2Br
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(3)在装置C中应加入c(填序号),其目的是吸收反应中可能生成的酸性气体.
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”“下”);
(5)安全瓶B中加入水,可以防倒吸,还可以检查反应进行时后面装置是否发生堵塞,写出发生堵塞时瓶B中现象:B中水面会下降,玻璃管中的水柱会上升,甚至溢出.
(6)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去;
(7)若产物中有少量副产物乙醚,可用蒸馏的方法除去.
 用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)有乙醇制备1,2-二溴乙烷的两个方程式:CH3CH2OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O、CH2=CH2+Br-Br→CH2Br-CH2Br
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(3)在装置C中应加入c(填序号),其目的是吸收反应中可能生成的酸性气体.
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”“下”);
(5)安全瓶B中加入水,可以防倒吸,还可以检查反应进行时后面装置是否发生堵塞,写出发生堵塞时瓶B中现象:B中水面会下降,玻璃管中的水柱会上升,甚至溢出.
(6)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去;
(7)若产物中有少量副产物乙醚,可用蒸馏的方法除去.
15.实验室用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
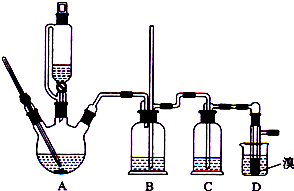
有关数据列表如下:
回答下列问题:
(1)写出该实验过程中发生的所有主要反应的化学方程式CH3CH2OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O、CH2=CH2+Br-Br→CH2Br-CH2Br.
(2)在此制各实验中,要尽可能迅速地把反应温度170℃左右,其最主要目的是d.(填正确选项前的字母,下同)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(3)在装置C中应加入c,其目的是吸收反应中可能生成的酸性气体.
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去(填实验现象).
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层
(6)若产物中有少量未反应的Br2,最好用b洗涤除去.
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(7)若产物中有少量副产物乙醚.可用蒸馏的方法除去.
(8)反应过程中应用冷水冷却装置D,其主要目的是冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
(1)写出该实验过程中发生的所有主要反应的化学方程式CH3CH2OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O、CH2=CH2+Br-Br→CH2Br-CH2Br.
(2)在此制各实验中,要尽可能迅速地把反应温度170℃左右,其最主要目的是d.(填正确选项前的字母,下同)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(3)在装置C中应加入c,其目的是吸收反应中可能生成的酸性气体.
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去(填实验现象).
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层
(6)若产物中有少量未反应的Br2,最好用b洗涤除去.
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(7)若产物中有少量副产物乙醚.可用蒸馏的方法除去.
(8)反应过程中应用冷水冷却装置D,其主要目的是冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.
20.高铁酸钠是一种新型、高效、多功能水处理剂,高铁酸钠(Na2FeO4)制备方法有:
湿法制备的主要反应为:2Fe(OH)3+3ClO-+4OH-═2FeO42-+3Cl-+5H2O,
干法制备的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法不正确的是( )
湿法制备的主要反应为:2Fe(OH)3+3ClO-+4OH-═2FeO42-+3Cl-+5H2O,
干法制备的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法不正确的是( )
| A. | 高铁酸钠中铁显+6价 | |
| B. | 湿法中每生成1 mol Na2FeO4转移3 mol电子 | |
| C. | 干法中每生成1 mol Na2FeO4转移4 mol电子 | |
| D. | Na2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3还能吸附水中的悬浮杂质 |
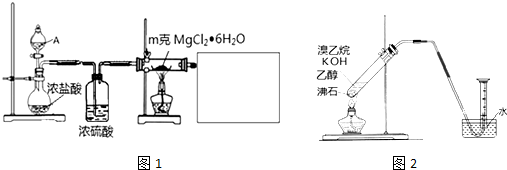
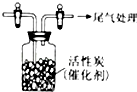 某学习小组推测SO2能与强氧化剂Cl2反应生成SO2Cl2,为此进行探究.
某学习小组推测SO2能与强氧化剂Cl2反应生成SO2Cl2,为此进行探究.