题目内容
7.下列各组元素中,电负性依次减小的是( )| A. | K、Na、Al | B. | O、Cl、H | C. | Si、P、H | D. | O、S、Cl |
分析 一般来说,周期表从左到右,元素的电负性逐渐变大;周期表从上到下,元素的电负性逐渐变小.电负性大得元素集中在元素周期表的右上角,电负性小的元素集中在左下角,以此解答该题.
解答 解:元素周期表中同周期元素从左到右元素的电负性逐渐增强,同主族元素从上到下元素的电负性逐渐减弱,
A.同主族元素从上到下,元素的电负性逐渐变小,则电负性Na>K,故A错误;
B.同主族元素从上到下,元素的电负性逐渐变小,同周期元素从左到右,元素的电负性逐渐变大,氧气可氧化氯离子,则电负性Cl>S,而O、Cl的电负性都大于H,所以电负性依次减小,故B正确;
C.同周期主族元素从左到右,元素的电负性逐渐增大,则电负性Si<P,故C错误;
D.同主族元素从上到下,元素的电负性逐渐变小,则电负性O>S;同周期元素从左到右,元素的电负性逐渐变大,则电负性Cl>S,所以先减小后增大,故D错误;
故选B.
点评 本题考查元素周期律知识,为高频考点,侧重于学生的分析能力的考查,本题注意把握元素周期律中电负性的递变规律即可解答,题目难度不大.

练习册系列答案
相关题目
17.乙酸正丁酯是无色透明有愉快果香气味的液体,可由乙酸和正丁醇制备.反应的化学方程式如下:
CH3COOH+CH2CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O
发生的副反应如下:2CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$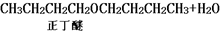
CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$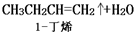
有关化合物的物理性质见表:
已知:乙酸正丁酯、正丁醇和水组成三元共沸物恒沸点为90.7℃.
合成:
方案甲:采用装置甲(分水器预先加入水,使水面略低于分水器的支管口),在干燥的50mL圆底烧瓶中,加入13.8mL(0.150mol)正丁醇和7.2mL(0.125mol)冰醋酸,再加入3~4滴浓硫酸和2g沸石,摇匀.按下图安装好带分水器的回流反应装置,通冷却水,圆底烧瓶在电热套上加热煮沸.在反应过程中,通过分水器下部的旋塞分出生成的水(注意保持分水器中水层液面仍保持原来高度,使油层尽量回到圆底烧瓶中).反应基本完成后,停止加热.
方案乙:采用装置乙,加料方式与方案甲相同.加热回流,反应60min后停止加热.
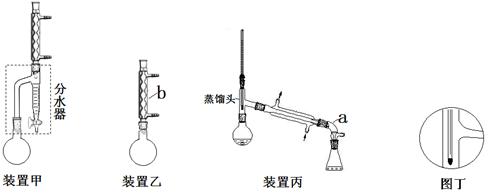
提纯:甲乙两方案均采用蒸馏方法.操作如下:

请回答:
(1)方案甲中使用分水器不断分离除去水的目的是有利于平衡向生成乙酸正丁酯的反应方向移动.
(2)仪器a的名称接受器或牛角管,仪器b的名称球形冷凝管.
(3)提纯过程中,步骤②的目的是为了除去有机层中残留的酸,步骤④加入少量无水MgSO4的目的是干燥.
(4)下列有关洗涤过程中分液漏斗的使用正确的是AB.
A.分液漏斗使用前必须要检漏,只要分液漏斗的玻璃塞和旋塞芯处不漏水即可使用
B.洗涤时振摇放气操作应如图所示

C.放出下层液体时,不需将要玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
D.洗涤完成后,先放出下层液体,然后继续从下口放出有机层置于干燥的锥形瓶中
(5)按装置丙蒸馏,最后圆底烧瓶中残留的液体主要是正丁醚;若按图丁放置温度计,则收集到的产品馏分中还含有正丁醇.
(6)实验结果表明方案甲的产率较高,原因是通过分水器及时分离出产物水,有利于酯化反应的进行,提高酯的产率.
CH3COOH+CH2CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O
发生的副反应如下:2CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$
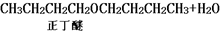
CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$
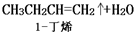
有关化合物的物理性质见表:
| 化合物 | 密度(g•cm-3) | 水溶性 | 沸点(℃) |
| 冰乙酸 | 1.05 | 易溶 | 118.1 |
| 正丁醇 | 0.80 | 微溶 | 117.2 |
| 正丁醚 | 0.77 | 不溶 | 142.0 |
| 乙酸正丁酯 | 0.90 | 微溶 | 126.5 |
合成:
方案甲:采用装置甲(分水器预先加入水,使水面略低于分水器的支管口),在干燥的50mL圆底烧瓶中,加入13.8mL(0.150mol)正丁醇和7.2mL(0.125mol)冰醋酸,再加入3~4滴浓硫酸和2g沸石,摇匀.按下图安装好带分水器的回流反应装置,通冷却水,圆底烧瓶在电热套上加热煮沸.在反应过程中,通过分水器下部的旋塞分出生成的水(注意保持分水器中水层液面仍保持原来高度,使油层尽量回到圆底烧瓶中).反应基本完成后,停止加热.
方案乙:采用装置乙,加料方式与方案甲相同.加热回流,反应60min后停止加热.

提纯:甲乙两方案均采用蒸馏方法.操作如下:

请回答:
(1)方案甲中使用分水器不断分离除去水的目的是有利于平衡向生成乙酸正丁酯的反应方向移动.
(2)仪器a的名称接受器或牛角管,仪器b的名称球形冷凝管.
(3)提纯过程中,步骤②的目的是为了除去有机层中残留的酸,步骤④加入少量无水MgSO4的目的是干燥.
(4)下列有关洗涤过程中分液漏斗的使用正确的是AB.
A.分液漏斗使用前必须要检漏,只要分液漏斗的玻璃塞和旋塞芯处不漏水即可使用
B.洗涤时振摇放气操作应如图所示

C.放出下层液体时,不需将要玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
D.洗涤完成后,先放出下层液体,然后继续从下口放出有机层置于干燥的锥形瓶中
(5)按装置丙蒸馏,最后圆底烧瓶中残留的液体主要是正丁醚;若按图丁放置温度计,则收集到的产品馏分中还含有正丁醇.
(6)实验结果表明方案甲的产率较高,原因是通过分水器及时分离出产物水,有利于酯化反应的进行,提高酯的产率.
2.“结晶玫瑰”具有强烈的玫瑰香气,是一种很好的定香剂.其化学名称为“乙酸三氯甲基苯甲酯”,通常用三氯甲基苯基甲醇和醋酸酐为原料制备:
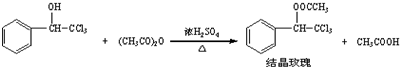
已知:
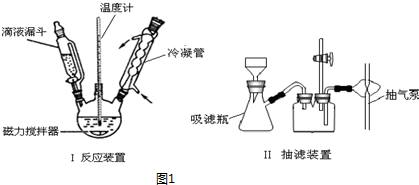
操作步骤和装置(图1)如下:
$\stackrel{加料}{→}$$→_{温度在110℃}^{加热3小时,控制}$$→_{入冰水中}^{反应液倒}$$\stackrel{抽滤}{→}$粗产品$\stackrel{重结晶}{→}$产品
请根据以上信息,回答下列问题:
(1)加料时,应先加入三氯甲基苯基甲醇和醋酸酐,然后慢慢加入浓硫酸并搅拌(或开启磁力搅拌器).待混合均匀后,最适宜的加热方式为油浴加热(填“水浴加热”,“油浴加热”,“砂浴加热”).
(2)用图II抽滤装置操作时,布氏漏斗的漏斗管插入单孔橡胶塞与吸滤瓶相接.橡胶塞插入吸滤瓶内的部分不得超过塞子高度的$\frac{2}{3}$;向漏斗中加入溶液,溶液量不应超过漏斗容量的$\frac{2}{3}$;当吸滤瓶中液面快达到支管口位置时,应拔掉吸滤瓶上的橡皮管,从吸滤瓶上口 倒出溶液.
(3)重结晶提纯时,应将粗产品溶解在无水乙醇中(填“水”,“无水乙醇”,“粗产品滤液”).已知70℃时100g 溶剂中溶解a g结晶玫瑰,重结晶操作过程为:按粗产品、溶剂的质量比为1:$\frac{100}{a}$混合,用水浴加热回流溶剂使粗产品充分溶解,然后待晶体完全溶解后停止加热(若溶液沸腾时还未全部溶解,可再加少量溶剂)冷却结晶,抽滤,此重结晶过程中不需要用到的仪器是c.
A.冷凝管 B.烧杯 C.蒸发皿 D.锥形瓶
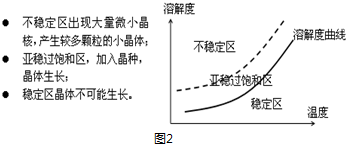
(4)某同学欲在重结晶时获得较大的晶体,查阅资料得到如图2信息:由信息可知,从高温浓溶液中获得较大晶体的操作为加入晶种,缓慢降温.
(5)在物质制备实验中,产品经抽滤、洗涤后,尚需干燥,请列举一种常见的实验室干燥方法.空气中风干、空气中晾干、高温烘干、用滤纸吸干.

已知:
| 三氯甲基苯基甲醇 | 无色液体.不溶于水,溶于乙醇. |
| 醋酸酐 | 无色液体.溶于水形成乙酸,溶于乙醇. |
| 结晶玫瑰 | 白色至微黄色晶体.不溶于水,溶于乙醇.熔点:88℃ |
| 醋酸 | 无色的吸湿性液体,易溶于水、乙醇. |
$\stackrel{加料}{→}$$→_{温度在110℃}^{加热3小时,控制}$$→_{入冰水中}^{反应液倒}$$\stackrel{抽滤}{→}$粗产品$\stackrel{重结晶}{→}$产品

请根据以上信息,回答下列问题:
(1)加料时,应先加入三氯甲基苯基甲醇和醋酸酐,然后慢慢加入浓硫酸并搅拌(或开启磁力搅拌器).待混合均匀后,最适宜的加热方式为油浴加热(填“水浴加热”,“油浴加热”,“砂浴加热”).
(2)用图II抽滤装置操作时,布氏漏斗的漏斗管插入单孔橡胶塞与吸滤瓶相接.橡胶塞插入吸滤瓶内的部分不得超过塞子高度的$\frac{2}{3}$;向漏斗中加入溶液,溶液量不应超过漏斗容量的$\frac{2}{3}$;当吸滤瓶中液面快达到支管口位置时,应拔掉吸滤瓶上的橡皮管,从吸滤瓶上口 倒出溶液.
(3)重结晶提纯时,应将粗产品溶解在无水乙醇中(填“水”,“无水乙醇”,“粗产品滤液”).已知70℃时100g 溶剂中溶解a g结晶玫瑰,重结晶操作过程为:按粗产品、溶剂的质量比为1:$\frac{100}{a}$混合,用水浴加热回流溶剂使粗产品充分溶解,然后待晶体完全溶解后停止加热(若溶液沸腾时还未全部溶解,可再加少量溶剂)冷却结晶,抽滤,此重结晶过程中不需要用到的仪器是c.
A.冷凝管 B.烧杯 C.蒸发皿 D.锥形瓶

(4)某同学欲在重结晶时获得较大的晶体,查阅资料得到如图2信息:由信息可知,从高温浓溶液中获得较大晶体的操作为加入晶种,缓慢降温.
(5)在物质制备实验中,产品经抽滤、洗涤后,尚需干燥,请列举一种常见的实验室干燥方法.空气中风干、空气中晾干、高温烘干、用滤纸吸干.
16.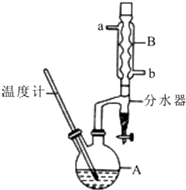 正丁醚常用作有机反应的溶剂.实验室制备正丁醚的反应和主要实验装置如下:2CH3CH2CH2CH2OH$?_{135℃}^{浓硫酸}$(CH3CH2CH2CH2)2O+H2O,反应物和产物的相关数据如表:
正丁醚常用作有机反应的溶剂.实验室制备正丁醚的反应和主要实验装置如下:2CH3CH2CH2CH2OH$?_{135℃}^{浓硫酸}$(CH3CH2CH2CH2)2O+H2O,反应物和产物的相关数据如表:
①将6mL浓硫酸和37g正丁醇,按一定顺序添加到A中,并加几粒沸石.
②加热A中反应液,迅速升温至135℃,维持反应一段时间.
③分离提纯:待A中液体冷却后将其缓慢倒入盛有70mL水的温度分液漏斗中,振摇后静置,分液得粗产物.
④粗产物依次用40mL水、20mL NaOH溶液和40mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙.
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11g.请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为:应先加正丁醇.
(2)加热A前,需先从b (填“a”或“b”)口向B中通入水.
(3)步骤③的目的是初步洗去浓H2SO4,振摇后静置,粗产物应上 (填“上”或“下”)口倒出.
(4)步骤⑤中,加热蒸馏时应收集D (填选项字母)左右的馏分.
A.100℃B.117℃C.135℃D.142℃
(5)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A.分水器中上层液体的主要成分为正丁醇,下层液体的主要成分为水.
(6)本实验中,正丁醚的产率为34% (精确到1%).
 正丁醚常用作有机反应的溶剂.实验室制备正丁醚的反应和主要实验装置如下:2CH3CH2CH2CH2OH$?_{135℃}^{浓硫酸}$(CH3CH2CH2CH2)2O+H2O,反应物和产物的相关数据如表:
正丁醚常用作有机反应的溶剂.实验室制备正丁醚的反应和主要实验装置如下:2CH3CH2CH2CH2OH$?_{135℃}^{浓硫酸}$(CH3CH2CH2CH2)2O+H2O,反应物和产物的相关数据如表:| 相对分子质量 | 沸点/℃ | 密度/(g/cm3) | 水中的溶解性 | |
| 正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
| 正丁醚 | 130 | 142.0 | 0.7704 | 几乎不容 |
②加热A中反应液,迅速升温至135℃,维持反应一段时间.
③分离提纯:待A中液体冷却后将其缓慢倒入盛有70mL水的温度分液漏斗中,振摇后静置,分液得粗产物.
④粗产物依次用40mL水、20mL NaOH溶液和40mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙.
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11g.请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为:应先加正丁醇.
(2)加热A前,需先从b (填“a”或“b”)口向B中通入水.
(3)步骤③的目的是初步洗去浓H2SO4,振摇后静置,粗产物应上 (填“上”或“下”)口倒出.
(4)步骤⑤中,加热蒸馏时应收集D (填选项字母)左右的馏分.
A.100℃B.117℃C.135℃D.142℃
(5)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A.分水器中上层液体的主要成分为正丁醇,下层液体的主要成分为水.
(6)本实验中,正丁醚的产率为34% (精确到1%).
17.天然气与二氧化碳在一定条件下反应制备合成气(CO+H2)的原理是CH4(g)+CO2(g)?2CO(g)+2H2(g)△H>0.该反应达到平衡之后,为了提高CH4的转化率,下列措施正确的是( )
| A. | 增大压强 | B. | 升高温度 | C. | 增大CH4浓度 | D. | 更换高效催化剂 |
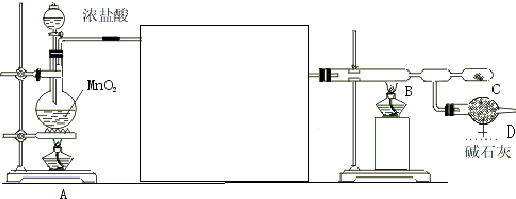
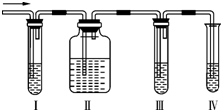 化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了如图所示的实验装置以确认上述混合气体中有C2H4和SO2.回答下列问题:
化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了如图所示的实验装置以确认上述混合气体中有C2H4和SO2.回答下列问题: