题目内容
15.浓硫酸和碳在加热的情况下反应的化学方程式为C+2H2SO4=CO2↑+2SO2↑+2H2O为了验证反应的各种生成物,用如图Ⅰ装置进行实验.
(1)图Ⅰ中A处是完成实验中的必要装置,它是下列图Ⅱ所示中的(填编号)③;

(2)C装置中应盛的试剂为足够酸性高锰酸钾溶液,其作用除去SO2;
(3)能够确定存在二氧化碳气体的实验现象C中酸性高锰酸钾溶液不褪色,同时D中澄清石灰水变混浊.
分析 根据题意可知浓硫酸与木炭共热生成CO2、SO2和H2O,反应的化学方程式为C+2H2SO4 $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;依次检验CO2、SO2和H2O的存在时,应先检验水蒸气的存在,因为在验证二氧化碳、二氧化硫的存在时都需通过溶液,可带出水蒸气;二氧化碳、二氧化硫都能使澄清的石灰水变浑浊,所以不能先通过澄清的石灰水来检验二氧化碳的存在,所以先检验二氧化硫的存在并除去二氧化硫后才检验二氧化碳的存在,据此答题.
解答 解:根据题意可知浓硫酸与木炭共热生成CO2、SO2和H2O,反应的化学方程式为C+2H2SO4 $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;依次检验CO2、SO2和H2O的存在时,应先检验水蒸气的存在,因为在验证二氧化碳、二氧化硫的存在时都需通过溶液,可带出水蒸气;二氧化碳、二氧化硫都能使澄清的石灰水变浑浊,所以不能先通过澄清的石灰水来检验二氧化碳的存在,所以先检验二氧化硫的存在并除去二氧化硫后才检验二氧化碳的存在,
(1)依次检验CO2、SO2和H2O的存在时,应先检验水蒸气的存在,因为在验证二氧化碳、二氧化硫的存在时都需通过溶液,可带出水蒸气;所以选择无水硫酸铜遇水变蓝验证水的生成,故答案为:③;
(2)二氧化碳、二氧化硫都能使澄清的石灰水变浑浊,所以不能先通过澄清的石灰水来检验二氧化碳的存在,所以先检验二氧化硫的存在并除去二氧化硫后才检验二氧化碳的存在,所以C装置中用高锰酸钾溶液除去二氧化硫,故答案为:酸性高锰酸钾溶液;除去SO2;
(3)由上述分析可知能够确定存在二氧化碳气体的实验现象是:C中酸性高锰酸钾溶液不褪色,同时D中澄清石灰水变混浊,
故答案为:C中酸性高锰酸钾溶液不褪色,同时D中澄清石灰水变混浊.
点评 本题考查了浓硫酸的性质应用产物的实验验证方法,明确三种气体的检验方法及检验的顺序是解决本题的关键.定性分析实验要求同学们根据实验现象进行分析处理,形成正确的结论.解题的关键在于收集的信息是否合理,对信息的处理是否正确等.

| A. | 在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA | |
| B. | 50mL18.4 mol/L浓硫酸与足量铜加热反应,生成SO2分子的数目为0.46NA | |
| C. | 1 molFe溶于过量硝酸,电子转移数为2NA | |
| D. | 78g Na2O2晶体中含有的离子数目为3NA |
C(金刚石,s)+O2(g)=CO2(g)△H=-395.41 kJ•mol-1;
C(石墨,s)+O2(g)=CO2(g)△H=-393.51 kJ•mol-1
则下列热化学方程式正确的是( )
| A. | C(石墨,s)=C(金刚石,s)△H=+1.9 kJ•mol-1; | |
| B. | C(石墨,s)=C(金刚石,s)△H=-1.9 kJ•mol-1; | |
| C. | C(石墨,s)=C(金刚石,s)△H=-788.92 kJ•mol-1; | |
| D. | C(石墨,s)=C(金刚石,s)△H=+788.92 kJ•mol-1; |
| A. | 滴加甲基橙试液显红色的溶液 Fe3+、NH4+、Cl-、SCN- | |
| B. | 水电离出来的c(H+)=10-13mol/L的溶液 K+、HCO3-、Br-、Ba2+ | |
| C. | pH值为1的溶液 Cu2+、Na+、Mg2+、NO3- | |
| D. | 所含溶质为Na2SO4的溶液 K+、HCO3-、NO3-、H+ |
| A. | 在pH=1的溶液中:NH+4、K+、CH3COO-、Cl- | |
| B. | 有SO42-存在的溶液中:Na+、Mg2+、Ba2+、I- | |
| C. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- | |
| D. | 在c(H+)=1.0×10-13mol•L-1的溶液中:Na+、S2-、AlO2-、SO32- |
| A. | CH3-CH=CH-COOH, | B. |  ,CH3CH2OH ,CH3CH2OH | ||
| C. |  ,HOCH2CH2OH ,HOCH2CH2OH | D. | CH3-CH=CH-COOH,CH3CH2OH |
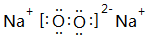 .
.