题目内容
3.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )| A. | 在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA | |
| B. | 50mL18.4 mol/L浓硫酸与足量铜加热反应,生成SO2分子的数目为0.46NA | |
| C. | 1 molFe溶于过量硝酸,电子转移数为2NA | |
| D. | 78g Na2O2晶体中含有的离子数目为3NA |
分析 A、氧气参与反应后可能变为+1价,也可能变为+2价;
B、铜只能和浓硫酸反应,和稀硫酸不反应;
C、铁和过量的硝酸反应后变为+3价;
D、求出过氧化钠的物质的量,然后根据过氧化钠中含2个钠离子和1个过氧根来分析.
解答 解:A、氧气参与反应后可能变为+1价,也可能变为+2价,故1mol氧气反应后得到的电子数可能为2NA个,故A错误;
B、铜只能和浓硫酸反应,和稀硫酸不反应,故浓硫酸不能反应完全,故生成的二氧化硫分子个数小于0.46NA个,故B错误;
C、铁和过量的硝酸反应后变为+3价,故1mol铁转移3NA个电子,故C错误;
D、78g过氧化钠的物质的量为1mol,而过氧化钠中含2个钠离子和1个过氧根,故1mol过氧化钠中含3NA个离子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
11.某化合物的化学式为C4H9Cl,它的可能的结构有几种( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
18.同主族两种元素原子的核外电子数的差值可能是( )
| A. | 6 | B. | 14 | C. | 26 | D. | 30 |
13.将O2、C、CO、CuO、NaHCO3、稀盐酸六种物质两两混合,有CO2生成的化学反应有( )
| A. | 3个 | B. | 4个 | C. | 5个 | D. | 6个 |
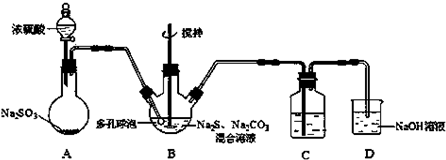


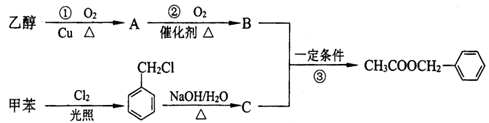
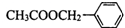 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下: