题目内容
4.我国拥有丰富的海洋资源,海水制盐历史悠久,早在5000年前的仰韶文化时期,先人就利用海水煮盐.为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):称取粗盐$\stackrel{①}{→}$ $→_{②}^{BaCl_{2}}$$→_{③}^{NaOH}$ $\stackrel{④}{→}$ $→_{⑤}^{过滤}$ 滤液$→_{⑥}^{适量盐酸}$ $→_{⑦}^{蒸发、结晶、烘干}$ 精盐
(1)第①步操作的名称是溶解,第②步判断BaCl2已过量的方法是取少量②中的上层清液于试管中,向其中滴加氯化钡溶液,若无白色沉淀生成,则证明氯化钡溶液已过量,反之未过量
(2)第④步加入试剂的化学式为Na2CO3.
(3)第⑤步操作所需玻璃仪器的名称是漏斗、烧杯、玻璃棒.
(4)若第⑤步、第⑥步顺序颠倒,将对实验结果产生影响,其原因是会有部分沉淀如CaCO3、BaCO3溶解,从而影响制得精盐的纯度.
分析 除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,加水溶解后,盐酸要放在最后,用于除去过量的氢氧化钠和碳酸钠,要先加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除过量的钡离子,即必须满足碳酸钠溶液应该在加入氯化钡溶液之后,盐酸必须在过滤之后加入,则②中加氯化钡可除去硫酸根离子,③中加NaOH除去镁离子,④中加碳酸钠可除去钡离子、钙离子,过滤后主要为氯化钠和碳酸钠,⑥中加盐酸反应后溶液中溶质为NaCl,然后蒸发结晶(剩余少量液体停止加热)得到NaCl,以此解答该题.
解答 解:除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,加水溶解后,盐酸要放在最后,用于除去过量的氢氧化钠和碳酸钠,要先加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除过量的钡离子,即必须满足碳酸钠溶液应该在加入氯化钡溶液之后,盐酸必须在过滤之后加入,则②中加氯化钡可除去硫酸根离子,③中加NaOH除去镁离子,④中加碳酸钠可除去钡离子、钙离子,过滤后主要为氯化钠和碳酸钠,⑥中加盐酸反应后溶液中溶质为NaCl,然后蒸发结晶(剩余少量液体停止加热)得到NaCl,
(1)在粗盐提纯之前要先将粗盐溶解于水中,第①步操作是溶解,钡离子和硫酸根离子会生成硫酸钡沉淀,BaCl2已过量,则再加氯化钡不会生成沉淀,则实验方法为:取第②步后的上层溶液1-2滴于点滴板上,再滴入1-2滴BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量,
故答案为:溶解;取少量②中的上层清液于试管中,向其中滴加氯化钡溶液,若无白色沉淀生成,则证明氯化钡溶液已过量,反之未过量;
(2)④中应加入Na2CO3,可除去钡离子、钙离子,故答案为:Na2CO3;
(3)过滤中用到的仪器有:铁架台、玻璃棒、烧杯、漏斗等,其中用到的三种玻璃仪器是漏斗、烧杯、玻璃棒;烧杯用来盛放液体,漏斗用于过滤,玻璃棒用来引流和搅拌.
故答案为:漏斗、烧杯、玻璃棒;
(4)若先用盐酸再进行操作⑤,盐酸可以将沉淀氢氧化镁、氢氧化铁、碳酸钙等溶解,从而影响制得精盐的纯度,
故答案为:会有部分沉淀如CaCO3、BaCO3溶解,从而影响制得精盐的纯度.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意离子检验及沉淀的洗涤,题目难度不大.

 阅读快车系列答案
阅读快车系列答案| A. | 用纯碱溶液清洗餐具上的油污 | B. | 用漂白液洗涤衣服上的字迹 | ||
| C. | 用稀硫酸清洗水壶里的水垢 | D. | 用汽油清洗皮肤上的油漆 |
| A. | Mn>Cu | B. | Al>Mn | C. | Mg>Al | D. | Mn>Mg |
| A. | 3个 | B. | 4个 | C. | 5个 | D. | 6个 |
| A. | 一定被氧化 | B. | 一定得到电子 | ||
| C. | 有可能被氧化,也有可能被还原 | D. | 一定由高价变为零价 |


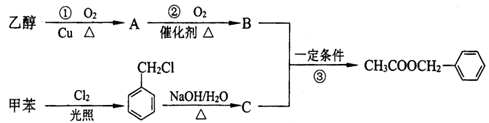
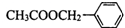 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下: