题目内容
6.对于反应A2(g)+3B2(g)=2C(g)+D(g)来说在四种不同情况下的反应速率分别为:①v(A)=0.15mol/(L•s)
②v(B)=0.6mol/(L•s)
③v(C)=0.5mol/(L•s)
④v(D)=0.45mol/(L•s)
则反应进行由快到慢的顺序为( )
| A. | ④>③>①>② | B. | ④>③>②>① | C. | ②>③>④>① | D. | ②>④>③>① |
分析 由化学反应速率与化学计量数成正比可知,反应速率与化学计量数的比值越大,反应速率越快,以此来解答.
解答 解:反应速率与化学计量数的比值越大,反应速率越快,则
①v(A)=0.15mol/(L•s),$\frac{0.15}{1}$=0.15;
②v(B)=0.6mol/(L•s),$\frac{0.6}{3}$=0.2;
③v(C)=0.5mol/(L•s),$\frac{0.5}{2}$=0.25;
④v(D)=0.45mol/(L•s),$\frac{0.45}{1}$=0.45,
则反应进行由快到慢的顺序为④>③>②>①,
故选B.
点评 本题考查化学反应速率与化学计量数的关系,为高频考点,把握速率与化学计量数比值法比较速率快慢为解答的关键,侧重分析与应用能力的考查,注意比值法应用,题目难度不大.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
1.木糖醇是一种新型的甜味剂,溶解性好,防龋齿,适合糖尿病患者的需要.其结构简式为:HOCH2(CHOH)3CH2OH.下列有关木糖醇的叙述中不正确的是( )
| A. | 木糖醇是一种单糖,不能发生水解反应 | |
| B. | 木糖醇不属于糖类,它是多元醇 | |
| C. | 木糖醇易溶解于水,能发生酯化反应 | |
| D. | 1mol木糖醇与足量钠反应最多可产生2.5molH2 |
11.如表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:①N,⑥Si,⑦S,⑪Ca.
(2)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar(用元素符号作答).
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是(填化学式)HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(4)在这些元素中(除稀有气体),原子半径最小的是(填元素符号)F,原子半径最大的是K.
(5)在⑤与④中,化学性质较活泼的是(填元素名称)镁,设计一个简单实验(只要写出实验方案即可),用化学实验证明.分别与水反应根据反应剧烈程度进行判断.
(6)在⑧与 ⑦中,单质的化学性质较活泼的是氯气,写出可以验证该结论的化学方程式Cl2+2H2S=2HCl+S↓.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar(用元素符号作答).
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是(填化学式)HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(4)在这些元素中(除稀有气体),原子半径最小的是(填元素符号)F,原子半径最大的是K.
(5)在⑤与④中,化学性质较活泼的是(填元素名称)镁,设计一个简单实验(只要写出实验方案即可),用化学实验证明.分别与水反应根据反应剧烈程度进行判断.
(6)在⑧与 ⑦中,单质的化学性质较活泼的是氯气,写出可以验证该结论的化学方程式Cl2+2H2S=2HCl+S↓.
18.有机物 的一氯代物可能的结构有(不考虑立体异构)( )
的一氯代物可能的结构有(不考虑立体异构)( )
 的一氯代物可能的结构有(不考虑立体异构)( )
的一氯代物可能的结构有(不考虑立体异构)( )| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
15.X是某元素的一种同位素,该原子的质量数为A,中子数为N,它的气态氢化物为XH3,则它与18O形成的最高价气态氧化物ag中含有质子的物质的量为( )
| A. | $\frac{a(A-N+3)}{A+3}$ | B. | $\frac{a(A-N+8)}{A+16}mol$ | ||
| C. | $\frac{a(2A-2N+40)}{2A+90}$ | D. | $\frac{2A-2N+24}{2A+54}mol$ |
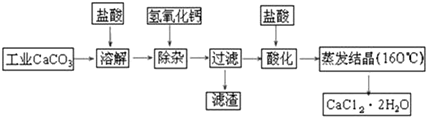
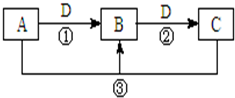 A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如图所示(部分反应中的H2O已略去).请填空:
A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如图所示(部分反应中的H2O已略去).请填空: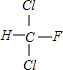 ;
;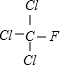 +HCl,生成氟氯昂可表示为F-11.
+HCl,生成氟氯昂可表示为F-11.