��Ŀ����
11�������Ԫ�����ڱ���һ���֣��ش������й����⣺| ������ ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | �� | �� | |
| 4 | �� | ⑪ | ⑫ |
��2������ЩԪ���У�����õĽ���Ԫ����K������õķǽ���Ԫ����F������õ�Ԫ����Ar����Ԫ�ط������𣩣�
��3������ЩԪ�ص�����������Ӧˮ�����У�������ǿ���ǣ��ѧʽ��HClO4��������ǿ����KOH�������Ե�����������Al��OH��3��
��4������ЩԪ���У���ϡ�����壩��ԭ�Ӱ뾶��С���ǣ���Ԫ�ط��ţ�F��ԭ�Ӱ뾶������K��
��5���ڢ�����У���ѧ���ʽϻ��õ��ǣ���Ԫ�����ƣ�þ�����һ����ʵ�飨ֻҪд��ʵ�鷽�����ɣ����û�ѧʵ��֤�����ֱ���ˮ��Ӧ���ݷ�Ӧ���ҳ̶Ƚ����жϣ�
��6���ڢ��� ���У����ʵĻ�ѧ���ʽϻ��õ���������д��������֤�ý��۵Ļ�ѧ����ʽCl2+2H2S=2HCl+S����
���� ��Ԫ�������ڱ���λ�ã���֪��ΪN����ΪF����ΪNa����ΪMg����ΪAl����ΪSi����S����ΪCl����ΪAr����ΪK��⑪ΪCa��⑫ΪBr��
��1���١��ޡ��ߡ�⑪�ֱ�ΪN��Si��S��Ca��
��2��ͬ����������ҽ����Լ������ǽ�������ǿ��ͬ�������϶��½�������ǿ���ǽ����Լ�����ϡ������ԭ�������Ϊ�ȶ��ṹ����ѧ������ܻ��ã�
��3���ǽ�����Խǿ����ۺ����������Խǿ��FԪ��û����ۺ����ᣬ�ʸ������������ǿ��������Խǿ������������Ӧˮ����ļ���Խǿ��������������Ե�������������
��4��ͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶����
��5��������У���ѧ���ʽϻ��õ�ΪMg����������ˮ��Ӧ�ľ��ҳ̶�˵����
��6������ ���У����ʵĻ�ѧ���ʽϻ��õ�Ϊ�����������õ���֮����û���Ӧ˵����
��� �⣺��Ԫ�������ڱ���λ�ã���֪��ΪN����ΪF����ΪNa����ΪMg����ΪAl����ΪSi����S����ΪCl����ΪAr����ΪK��⑪ΪCa��⑫ΪBr��
��1���١��ޡ��ߡ�⑪�ֱ�ΪN��Si��S��Ca���ʴ�Ϊ��N��Si��S��Ca��
��2��ͬ����������ҽ����Լ������ǽ�������ǿ��ͬ�������϶��½�������ǿ���ǽ����Լ�����������Ԫ��������õĽ���Ԫ���Ǣ⣬ΪKԪ�أ�����õķǽ���Ԫ���Ǣڣ�ΪFԪ�أ�����õ�Ԫ���ǢᣬΪAr��
�ʴ�Ϊ��K��F��Ar��
��3���ǽ�����Խǿ����ۺ����������Խǿ��FԪ��û����ۺ����ᣬ��HClOH4��������ǿ��������Խǿ������������Ӧˮ����ļ���Խǿ����KOH�ļ�����ǿ��Al��OH��3�������������
�ʴ�Ϊ��HClO4��KOH��Al��OH��3��
��4��ͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶����ԭ�Ӱ뾶��С����F��ԭ�Ӱ뾶������K���ʴ�Ϊ��F��K��
��5��Mg��Al������ͬ����Ԫ�ؽ����Եĵݱ���ɿ�֪��������Mg��Al�������жϽ�����ǿ���ķ����������ݶ��ߵ��ʷֱ���ˮ��Ӧ�ľ��ҳ̶����ж��������ǿ����
�ʴ�Ϊ��þ���ֱ���ˮ��Ӧ���ݷ�Ӧ���ҳ̶Ƚ����жϣ�
��8����͢߷ֱ���Cl��S������ͬ����Ԫ�طǽ����Եĵݱ���ɿ�֪���ǽ�����Cl��S�������жϷǽ�����ǿ���ķ����������ݶ�����̬�⻯����ȶ��ԡ�����֮����û���Ӧ�����ж���ǽ�����ǿ������Cl2+2H2S=2HCl+S����
�ʴ�Ϊ��������Cl2+2H2S=2H++2Cl-+S����
���� ���⿼��Ԫ��λ�á��ṹ�����ʵĹ�ϵ��Ϊ��Ƶ���㣬����Ԫ�ص�λ�á�Ԫ�ص����ʼ�Ԫ��������Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��Ԫ�������ɼ�Ԫ�ػ�����֪ʶ���ۺ�Ӧ�ã���Ŀ�ѶȲ���

| A�� | ���Ƽ���Cu��OH��2����Һ | B�� | FeCl3��Һ | ||
| C�� | BaCl2��Һ | D�� | ����KMnO4��Һ |
��֪�������������������pH
| Mn��OH��2 | Fe��OH��2 | Fe��OH��3 | Cu��OH��2 | |
| ��ʼ����ʱ | 8.3 | 6.3 | 2.7 | 4.7 |
| ��ȫ����ʱ | 9.8 | 8.3 | 3.7 | 6.7 |
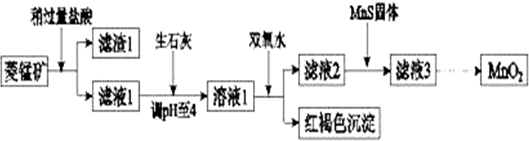
��1�������ʵ����̿�ʹ��ǰ�轫����飬��ҪĿ��������Ӵ��������߷�Ӧ���ʣ������ܽ�MnCO3�Ļ�ѧ����ʽ��MnCO3+2HCl=MnCl2+CO2��+H2O��
��2������Һ1�м���˫��ˮʱ����Ӧ�����ӷ���ʽ��2Fe2++H2O2+4H2O=2Fe��OH��3��+4H+��
��3����Һ2�м����Թ��������ܵ����MnS���Գ�ȥCu2+����Ӧ�����ӷ���ʽ��MnS+Cu2+=Mn2++CuS��
��4����MnCl2ת��ΪMnO2��һ�ַ���������������������������ữ��NaClO3��Һ��MnCl2�������÷�Ӧ�����ӷ���ʽΪ����Mn2++��ClO3-+��4H2O=��Cl2+��5MnO2+��8H+��
��5����MnCl2ת��ΪMnO2����һ�ַ����ǵ�ⷨ��
����������MnO2�ĵ缫��Ӧʽ��Mn2+-2e-+2H2O=MnO2+4H+��
����ֱ�ӵ��MnCl2��Һ������MnO2��ͬʱ���������Cl2������Cl2�IJ����ǽ���ʪ�ĵ��۵⻯����ֽ������������������ֽ������֤����Cl2���ɣ�
����������MnCl2��Һ�м���һ������Mn��NO3��2��ĩ������Cl2��������ԭ�����������������£�����Mn2+Ũ�Ȼ�����$\frac{c��M{n}^{2+}��}{c��C{l}^{-}��}$��������Mn2+�ŵ磨������Cl-�ŵ磩����
��v��A��=0.15mol/��L•s��
��v��B��=0.6mol/��L•s��
��v��C��=0.5mol/��L•s��
��v��D��=0.45mol/��L•s��
��Ӧ�����ɿ쵽����˳��Ϊ��������
| A�� | �ܣ��ۣ��٣��� | B�� | �ܣ��ۣ��ڣ��� | C�� | �ڣ��ۣ��ܣ��� | D�� | �ڣ��ܣ��ۣ��� |
| A�� | 20Ne��22Ne��Ϊͬλ�� | B�� | Һ�Ⱥ���ˮ��ͬһ������ | ||
| C�� | ���ʯ��ʯī��Ϊͬ���칹�� | D�� | �ⵥ�ʺ͵�������Ϊͬ�������� |
| A�� | C2H6 | B�� | C4H8 | C�� | C2H6O | D�� | C6H12O6 |
 ��ѧ���ѻ���˼��������о������N4���ӣ���ṹΪ�������壨��ͼ��ʾ��������������ƣ���̬ʱ����֪����1mol N-N������167kJ����������1mol N��N������942kJ������������
��ѧ���ѻ���˼��������о������N4���ӣ���ṹΪ�������壨��ͼ��ʾ��������������ƣ���̬ʱ����֪����1mol N-N������167kJ����������1mol N��N������942kJ������������| A�� | N4��N2����Ϊͬλ�� | |
| B�� | N4����һ�����͵Ļ����� | |
| C�� | N4��ѧ���ʱ�N2�ȶ� | |
| D�� | 1mol N4����ת��ΪN2ʱҪ�ų�882kJ���� |
| A�� | 25��ʱ��pH=7��NH4Cl��NH3•H2O�����Һ�У�����OH-����ĿΪ10-7NA | |
| B�� | һ��������6.4gSO2������������Ӧ��ת�Ƶĵ�����Ϊ0.2NA | |
| C�� | ����3NA�����ӵ�Na2O2��������ˮ���1L��Һ��������Һ��Na-��Ũ��Ϊ2mol•L-1 | |
| D�� | 46gC2H4O�к��е�C-H����Ŀһ��Ϊ5NA |
